研究人员朝着遗传性失明的新疗法迈出了关键一步
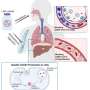
俄勒冈州立大学药学院的科学家们在动物模型中证明了使用脂质纳米颗粒和信使RNA (COVID-19疫苗的基础技术)治疗与罕见遗传疾病相关的失明的可能性。
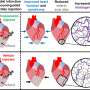
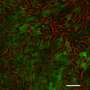
研究人员开发了能够穿透神经视网膜并将mRNA传递给感光细胞的纳米颗粒,这些感光细胞的正常功能使视觉成为可能。
这项研究由俄勒冈州立大学药剂学副教授Gaurav Sahay,俄勒冈州立大学博士生Marco Herrera-Barrera和俄勒冈健康与科学大学眼科助理教授Renee Ryals领导,于今天发表在《柳叶刀》杂志上科学的进步.
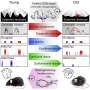
科学家们克服了使用上的主要限制脂质纳米粒子,或LNPs,来携带遗传物质为了视觉治疗的目的——让它们到达眼睛后部,也就是视网膜所在的地方。
脂类是脂肪酸和类似的有机化合物,包括许多天然油和蜡。纳米颗粒是一种微小的物质,大小从一米的十亿分之一到1000亿分之一米不等。信使RNA向细胞传递制造特定蛋白质的指令。
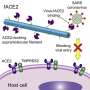
对于冠状病毒疫苗,LNPs携带的mRNA指示细胞制造病毒刺突蛋白的无害片段,从而触发身体的免疫反应。作为一种治疗由遗传性视网膜退化(IRD)引起的视力损害的疗法,这种信使rna会指示因基因突变而出现缺陷的感光细胞制造视力所需的蛋白质。
IRD包括一组不同严重程度和患病率的疾病,全世界每几千人中就有一人患有这种疾病。
科学家们在涉及小鼠和动物的研究中表明非人灵长类动物研究人员发现,含有多肽的LNPs能够穿过眼睛中的屏障,到达神经视网膜——在那里光被转化为电信号,大脑将其转化为图像。
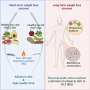
“我们发现了一组新的肽,可以到达眼睛的后部,”Sahay说。“我们使用这些肽来充当邮政编码将携带遗传物质的纳米颗粒运送到眼睛内的预定地址。”
“我们发现的肽可以作为直接与沉默rna结合的靶向配体,小分子用于治疗或成像探针,”Herrera-Barrera补充道。
Sahay和Ryals已经从国家眼科研究所获得了320万美元的资助,继续研究脂质纳米颗粒在治疗遗传性失明方面的前景。他们将领导研究使用LNPs提供基因编辑工具,可以删除基因中的坏基因感光细胞然后用功能正常的基因替换它们。
该研究旨在为目前基因编辑的主要传输手段(一种被称为腺相关病毒(AAV)的病毒)的局限性开发解决方案。
Sahay说:“与LNPs相比,AAV的包装能力有限,它可以引发免疫系统反应。”“在继续表达编辑工具用作分子剪刀在待编辑DNA上切割的酶方面,它也做得不太好。我们希望利用迄今为止我们对LNPs的了解来开发一种改进的基因编辑器传递系统。”
更多信息:肽引导的脂质纳米颗粒将mRNA传递到啮齿动物和非人灵长类动物的神经视网膜,科学的进步(2023)。DOI: 10.1126 / sciadv.add4623.www.science.org/doi/10.1126/sciadv.add4623