说,新的分子拦截器停止乳腺癌转移的研究
估计有百分之九十的人死于乳腺癌是由于转移带来的并发症,这一过程中,肿瘤细胞脱离,他们首先形成,通过血液或淋巴循环系统,并形成新的转移性肿瘤在身体的其他部位。
没有有效的治疗阻止这一过程,不仅需要目标原发肿瘤侵入时,而且其转移潜力类型的乳腺癌和/或在一个高级阶段被诊断出乳腺癌。
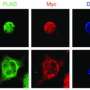
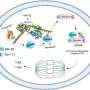
癌细胞使用脚突起叫invadopodia降低底层组织,进入血液和形式在其他器官转移。大约四年前有Gil-Henn博士和Azrieli医学院的研究人员透露以色列巴伊兰大学两个重要线索invadopodia的形成:蛋白质Pyk2和cortactin可疑的细胞水平增加时,细胞进入恶性阶段,但当细胞生成Pyk2失去了能力,没有任何观察转移。
在最近的一项研究中扩大这一发现,Gil-Henn博士和教授乔丹寒意,保存期的化学系,这些伴侣蛋白之间的相互作用特征,表明这种交互是转移形成的先决条件癌症细胞。
进一步,他们决定的机制cortactin-Pyk2交互影响invadopodia形成和定义这两个蛋白质之间的复杂的结构。研究小组的结果,也包括沙姆斯Twafra博士和长安汽车Sokolik,发表在《华尔街日报》致癌基因。
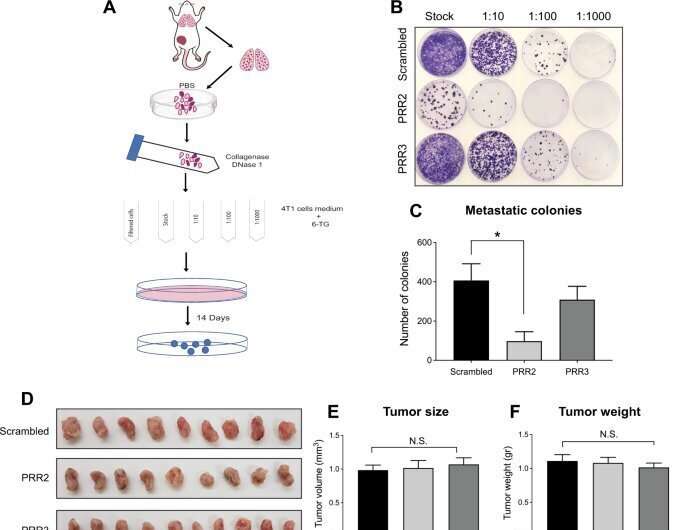
在最近的研究中研究者定义精确的蛋白质参与Pyk2之间的交互和cortactin。小段,称为肽,在实验室合成和管理乳房cancer-bearing老鼠。成功合成肽与自然Pyk2蛋白质争夺的“关注”cortactin基本上阻塞Pyk2的访问。这种抑制的形成脚invadopodia,因此,小鼠的肺保持更健康,很少,如果有的话,转移。
“我们非常兴奋地看到,使用Pyk2-binding主题cortactin作为invadopodia抑制剂在体内很好,”研究的合著者有Gil-Henn博士说。“这证明了临床潜在抑制新发现的互动。”
令人惊讶的是,所有这一切都是通过使用一个非常小的一部分Pyk2,跨越只有19的1009氨基酸构建块。这是看到的,如上所述,在降低乳腺癌肺转移的小鼠模型。此外,它大大减少乳腺肿瘤细胞的侵袭性,停止invadopodia成熟的肿瘤细胞,降低了肌动蛋白的聚合速度,需要在invadopodia形成发展。所有这些发现提供了明确的证据表明,19-amino酸肽实际上块转移。
教授乔丹寒意,专攻确定蛋白质的三维结构,加入了研究团队来确定肽块转移。
“开发一个成功的药物的抑制肽极其苛刻,几乎是不可能不完整的肽之间的复杂的结构视图和它的目标,在这种情况下cortactin,”教授说的严寒。通过核磁共振实验称为NOESY,每个的881个原子的位置cortactin蛋白质和肽测定的315个原子,创建一个三维的结构。
原子的空间位置的秘密理解蛋白质之间的键的强度,这是至关重要的建立一个药物能有效防止债券。为了说明这一点,发现氨基酸肽完全符合的# 10 cortactin“槽”,不能改变,而氨基酸# 11面临外在和它的确切身份不那么重要了。
Gil-Henn博士和教授寒意现在专注于将肽转换成一个更好的候选药物。不同序列的氨基酸生产出的产品,测试将提供一个更强大和更具体的绑定cortactin的目标站点。特异性是至关重要的,因为网站在cortactin绑定,称为SH3,类似于其他蛋白质SH3网站,任何不必要的绑定到另一个地方蛋白质可能会引起副作用。
两种蛋白质的结合细胞生物学(发现和显示,我们可以有效地阻止转移)和结构生物学(给我们的如何以及为什么绑定事件)带来科学曾经如此接近乳房而战癌症在某种程度上不可能。研究人员希望这种进步会导致药物抑制转移形成的发展,并将成为可用的治疗方法来改善生存机会和侵入性诊断病人的生活质量乳腺癌和其他转移性癌症。
更多信息:Shams Twafra et al,小说Pyk2-derived肽抑制invadopodia-mediated乳腺癌转移,致癌基因(2022)。DOI: 10.1038 / s41388 - 022 - 02481 - w