研究确定了原发性乳腺癌和转移性乳腺癌之间的分子差异
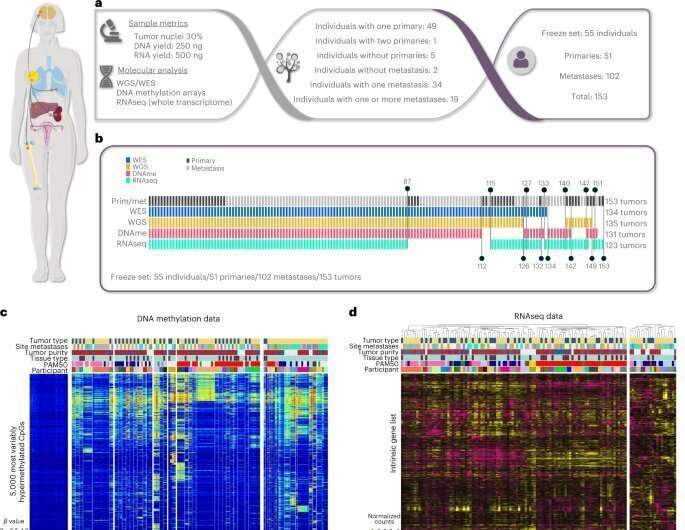
一项多机构的全国性研究已经确定了导致转移性乳腺癌发展和进展的独特分子特征。其中一个关键特征涉及免疫系统的变化,部分原因是HLA-A基因的甲基化;甲基化是在DNA分子上加上一个小的化学基团。也发现了局部缺失,或部分HLA-A基因的丢失,并且与DNA甲基化的样本相互排斥。在这项研究中,甲基化和局灶性缺失导致更少的免疫细胞可用来攻击癌细胞。
研究结果发表于2022年12月30日自然癌症.
这项由AURORA US转移网络项目领导的研究,是首批使用多个基因组平台来分析原发性(原始)肿瘤及其配对肿瘤的研究之一转移;大多数早期研究都是孤立地观察原发癌或转移癌。在这项针对55名女性的新研究中转移性乳腺癌,研究人员收集了代表51种原发癌症和102种成对转移的肿瘤组织。
“这项研究涉及许多机构的广泛合作,以促进我们对乳腺癌的了解,”查尔斯·m·佩罗博士说,他是分子肿瘤学的May Goldman Shaw杰出教授,北卡罗来纳大学莱因伯格综合癌症中心乳腺癌研究项目的联合负责人,也是这项研究的通讯作者。“我们对乳腺癌生物学的了解来自于对原发肿瘤的研究,但当人们死于乳腺癌时,它是死于转移性疾病,所以我们对转移性生物学的缺乏理解阻碍了对患者的护理。”
研究人员发现T细胞和B细胞在很大程度上直接抗肿瘤免疫反应的转移明显较少。他们还观察了不同转移部位之间的差异;与肺转移相比,肝和脑转移的免疫细胞反应水平较低。
“我们发现,大约17%的转移性肿瘤影响细胞免疫的基因表达减少,免疫细胞渗透环境和抵抗的能力下降癌症细胞苏珊娜·加西亚-雷西奥博士说,她是北卡罗来纳大学莱因伯格分校佩鲁实验室的助理教授,也是这项研究的联合主要作者。
除了Garcia-Recio,这篇论文的其他共同主要作者是Toshinori Hinoue博士,密歇根州大急流城的Van Andel研究所;Gregory L. Wheeler博士和Benjamin J. Kelly女士,来自俄亥俄州哥伦布市的全国儿童医院;Ana C. Garrido-Castro,波士顿Dana-Farber癌症研究所医学博士。
“这一发现只代表了AURORA美国转移网络项目的前半部分,因为研究人员最近启动了一项临床试验,以帮助收集更多的样本,”西雅图弗雷德·哈金森癌症中心临床事务执行副总裁南希·e·戴维森医学博士说,她也是AURORA的创始人之一。“试验样本的分析结果将添加到当前数据中,从而能够更好地检测基因组变化,从而真正增强我们对疾病的理解。”
“我们在大约30%的患者中看到了生物学上的变化,包括免疫激活的丧失,特别是在肝和脑转移中,”丽莎·a·凯莉(Lisa A. Carey)说,医学博士,ScM, FASCO,临床科学副主任,以及北卡罗来纳大学莱恩伯格分校(UNC Lineberger)乳腺癌研究的L.理查森和玛丽莲·雅各布斯·普雷耶(Marilyn Jacobs Preyer)杰出教授和研究作者。“其中许多变化是通过可以逆转或治疗的机制发生的。因此,基于这一努力,我们对改善转移性疾病治疗,甚至预防转移本身的潜力感到非常兴奋。”
乳腺癌研究基金会创始科学主任Larry Norton医学博士说:“这项至关重要的研究——它确定了一个潜在的控制转移性疾病的新靶点——证明了由献身于重要使命的人们团结起来进行广泛合作研究的价值。”
Perou说:“我们非常感谢我们的患者帮助我们推进这些研究工作,并感谢他们在未来做出的任何贡献。”“我们目前正在我们的小鼠模型中模仿大量这些遗传发现,我们正在测试新的治疗方法,并取得了真正的进展,我们希望在不久的将来能为患者带来回报。”