基因分离的力量:数以百计的小说基因发现
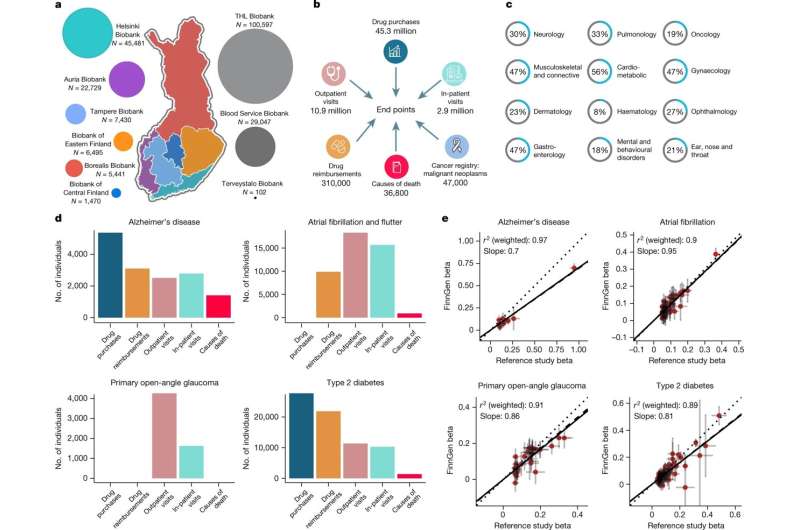
新结果FinnGen研究财团的演示芬兰的不可否认的好处为基因组研究卫生研究的环境。在小说的财富基因发现未知的遗传风险因素对许多退行性疾病。这些发现有潜在促进新疗法的发展。
自2017年启动以来,FinnGen研究已经发展成为一个世界领先的biobank-based基因组研究项目。目前FinnGen完成资源整合基因组信息的建设从500000年芬兰人有超过半个世纪的国家卫生注册表数据。
FinnGen旗舰的研究,只是发表在自然,是一个令人信服的芬兰独有的健康数据演示的机会,人口结构、立法框架和生物组织,结合其他地方存在。
这里FinnGen团队描述结果基于224737名芬兰生物参与者。执行全面的基因分析之后超过1900种疾病,研究人员确定近2500基因组区域与至少一种疾病。
“即使不到一半的招募了500000名参与者在这个阶段,分析本快照的结果描述FinnGen财富重要基因的发现,包括小说和保护变异常见和风险罕见疾病FinnGen科学主任,说:“教授Aarno Palotie分子医学研究所的芬兰菲、赫尔辛基大学。
芬兰的卫生注册和生物银行提供独一无二的机会
在芬兰,健康信息,如医疗诊断,手术和药物处方捕获几十年来在国家电子健康记录整个人口。这创造了独特的研究机会。
旗舰出版物,等熟练的利用团队首先表明注册数据,研究参与者的健康历史可以可靠地创作和研究。为此,作者比较FinnGen结果与早期基因发现15之前被充分研究过的常见疾病,如2型糖尿病、哮喘和阿尔茨海默氏症。
除了验证注册数据的有效性,研究人员表明,识别新的风险变异FinnGen可能数量小得多的患者相比,最大的发表针对疾病的基因研究。
“芬兰健康寄存器包含健康和药物数据与一个人的一生,让我们迅速和准确地识别疾病病例。这个精确的表现型,加上芬兰人口的历史是一个非常强大的组合对小说在各种各样的疾病基因的发现,”博士评论Mitja库凯山,这项研究的第一作者从麻省理工和哈佛和赫尔辛基大学。
新的入口点进入疾病生物学
芬兰独特的地理位置和语言隔离,芬兰人有明显的祖先可以追溯到一个小成立人口大约100 - 150代。因此,现代芬兰人口,尽管大致类似于欧洲人的基因,有一个不寻常的和大量的遗传变异不经常发现在世界其他地方。几百2500年疾病相关变异研究中描述的这一类。
在这些变量中,研究人员强调29日,位于基因未与任何疾病。一个例子是一个变异的基因称为TNRC18诱发炎症性肠病和其他炎症条件。其他的例子包括变异增加甲状腺功能减退的风险,听力损失或子宫内膜异位,从关节和变异,提供保护,青光眼或心脏疾病。
“这些发现表明人口瓶颈找到入口点的力量为常见疾病的生物学变异相当罕见,但有强烈的生理影响,”马克说戴利,分子医学研究所的主任芬兰赫尔辛基大学的菲,这项研究背后的领导机构。
额外FinnGen本周发表的论文提供了有趣的发现的例子,增加我们的理解基因预测药物的使用模式,以及机制导致耳硬化症和呼吸道感染、其他疾病。此外,另一个FinnGen发表在同一期自然强调了古典继承模型传统上认为在基因组研究和临床诊断不能完全捕捉遗传效应的范围在人群中观察到。
的一个独特方面FinnGen除了公共资金支持FinnGen 13制药公司和有共同的科学方向学术和行业合作伙伴。因此FinnGen研究理想的位置,可以解决基础研究问题有可能影响治疗的开发和交付。
“这个新的信息,芬兰人口的遗传组成现在毫无疑问在世界上最著名的。然而,我们的研究的影响更广泛,无处不在,能帮助患者“Palotie教授说。
更多信息:Aarno Palotie, FinnGen从井提供的见解独特的遗传表型孤立的人口,自然(2023)。DOI: 10.1038 / s41586 - 022 - 05473 - 8。www.nature.com/articles/s41586 - 022 - 05473 - 8