科学家精确定位了新冠病毒在我们鼻子内的进出端口
刚才有人对着你咳嗽。在飞机上。在一个晚宴上。在超市排队时。
要是有个“事后早晨”就好了喷鼻剂这可能会摧毁呼吸道病毒在你鼻子和喉咙上的殖民能力。
在1月5日出版的一项研究中细胞斯坦福大学病理学、微生物学和免疫学教授彼得·杰克逊博士和他的同事们通过精确定位SARS-CoV-2 (COVID-19病毒)进入和离开我们鼻腔细胞的途径,使这种可能性更接近现实。杰克逊说:“我们的上呼吸道不仅是肺部感染的发射台,也是传播给他人的发射台。”
杰克逊与加州大学旧金山分校微生物学和免疫学教授劳尔·安迪诺博士共同参与了这项研究,这是首次从分子细节上描述COVID-19鼻腔感染。该研究的主要作者是前斯坦福大学医学博士后学者吴建廷博士和研究生程然,以及加州大学旧金山分校博士后学者Peter Lidsky博士和Yinghong Xiao博士。
一条河穿过它
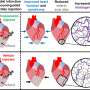
鼻子和气道都有上皮组织主要由三部分组成细胞类型:基底细胞,杯状细胞还有多纤毛细胞,占鼻上皮细胞总数的80%。多纤毛细胞形成保护屏障,防止病毒进入气道。
Jackson和他的同事们放大了在多纤毛上皮细胞上发现的两种结构:纤毛和微绒毛。虽然这两种结构都是众所周知的,但之前还没有发现这两种结构与病毒如何进入或离开气道内的细胞有关。
纤毛是各种细胞向外表面生长的意大利面状附属物。单个鼻上皮细胞上可能有多达400条这样的鞭状链鼻腔-面表面,所有持续跳动和谐。它们的顶部是一层薄薄的蛋白质,叫做黏液——与黏液中的关键蛋白质密切相关——在其上面是一层黏液。
杰克逊说,黏蛋白分子可以相互连接,形成类似于弹性三维链状栅栏的网状结构,防止SARS-CoV-2等较大的病毒进入上呼吸道细胞。粘液被包裹住了病毒颗粒、细菌、环境碎片和细胞分解垃圾,并保持底层细胞湿润。
上呼吸道上皮纤毛穿过这层黏液,它们同步的搏动产生一种波,推动黏液及其被包裹的颗粒,就像一条缓慢流动的河流,到可以咳出或被吞咽和消化的地方。
几乎所有动物细胞的另一个共同特征是微绒毛,从细胞表面延伸出来的小刺,就像小手指一样。微绒毛可以抓取和运输亚细胞颗粒和囊泡。
你说再见,我说你好
为了近距离观察病毒感染初期发生了什么,杰克逊和他的同事们使用了一种复杂的组织培养方法来产生他们所谓的气道上皮类器官,它模拟正常的气道。而缺乏血管和免疫细胞,这些类器官完全概括了鼻上皮的结构,包括完整的黏液-黏液层和发育良好的多缘细胞。
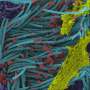
科学家们将这些培养物与SARS-CoV-2放在同一个培养皿中进行接种。用光和电子显微镜免疫化学染色,他们监测上皮细胞的病毒进入,复制和退出。
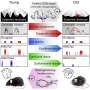
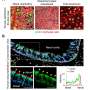
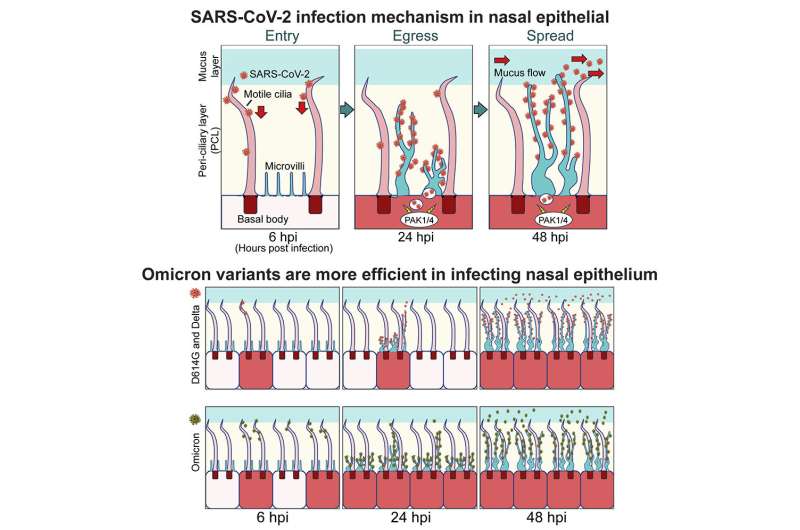
只有纤毛细胞被感染。电子显微镜显示病毒最初只附着在纤毛上。在类器官与SARS-CoV-2孵育6小时后,许多病毒颗粒从顶端往下散布在纤毛的两侧。即使接种24小时后,病毒也只在少数细胞中复制。大规模复制需要48小时。
SARS-CoV-2在现实生活中也需要整整一两天才能开始全面复制。
通过降低鼻腔上皮细胞中对纤毛形成至关重要的蛋白质水平,纤毛被耗尽,严重减缓了SARS-CoV-2感染。
杰克逊说:“很明显,人类纤毛鼻上皮细胞是SARS-CoV-2进入鼻上皮组织的主要部位。”
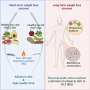
研究人员怀疑感染的延迟是由于病毒必须通过气道黏液-粘蛋白屏障,他们用一种粘蛋白选择性酶处理气道类器官,这种酶可以分解粘蛋白网络网格。杰克逊说,它在24小时内加速了病毒的进入,从“几乎无法检测到”到“很容易检测到”,他的结论是,消除这种网状物中的粘蛋白可以阻止网状物阻止类器官的SARS-CoV-2感染。
在患有原发性纤毛运动障碍的罕见疾病的患者中,他们的纤毛搏动能力受损或不再同步,粘液流动失去了方向性。
在这些患者产生的气道类器官中,病毒附着在纤毛上的情况与正常细胞相似。接种24小时后,细胞侵染率与正常感染细胞相似。看起来正常的微绒毛竖立在细胞表面。
但在48小时后,SARS-CoV-2感染的细胞总数要少得多——它只能感染周围的细胞——这表明,一旦SARS-CoV-2开始在被感染的细胞内复制,病毒依靠充足的粘液流动来帮助它在整个上呼吸道传播。
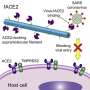
2020年5月A自然通讯杰克逊参与撰写的这项研究表明,ace2 -典型的sars - cov -2结合细胞表面分子或受体-集中在鼻上皮细胞的纤毛上。新细胞研究表明,SARS-CoV-2通过该受体与上皮纤毛结合。
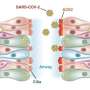
杰克逊说,从那里,病毒可能以以下两种方式之一滑过黏液-黏液屏障:一种是跳房子式地从纤毛一侧跳下来,从一个ACE2分子跳到下一个分子,直到到达细胞的主体,在那里与细胞膜融合并爬进去;或者通过插入纤毛,乘坐内部货运电梯到达细胞体。
“一旦病毒通过了这道屏障,”他说,“它就可以在底层细胞中自由复制。”
研究人员还发现,SARS-CoV-2一旦进入细胞,就会诱导细胞内酶的活动,导致微绒毛扩大和分枝,就像疯狂的仙人掌植物一样,直到它们的尖端伸出粘液屏障之上。他们的数量在增加。接种疫苗24小时后,许多改变的微绒毛,通常不到纤毛的一半长度,已经变成了巨大的、分枝的、树状的结构,有纤毛的大小或更大,它们被附着的病毒颗粒装饰着,这些病毒颗粒可以进入黏液-黏液层,在那里它们可以沿着黏液河漂流,感染其他更远的细胞。
研究人员在细胞中精确定位了由SARS-CoV-2感染大量开启的酶,这些酶导致了微绒毛的转化。抑制这些酶使这种变异停止,并大大减少了病毒向其他细胞的传播。
一剂喷雾就能把他们都绑起来?
Jackson和他的同事将呼吸道类器官与另外两种呼吸道病毒(现在激增的呼吸道合胞病毒和不太常见的副流感病毒)中的任何一种孵卵,以及BA.1(一种omicron菌株的变种),得到了类似的结果。
Omicron的传染性更强,正如预期的那样,它比用于其他SARS-CoV-2实验的旧菌株更快地感染呼吸道器官多纤毛细胞。但抑制病毒进入或退出气道细胞仍然被证明是有效的,即使是对这种高传染性变异。
Jackson说,这些病毒进入机制可能是许多呼吸道病毒的普遍特征。
这一发现为一种鼻用药物确定了新的靶点,这种药物通过阻止纤毛运动或微绒毛肥大,甚至可以防止未知的呼吸道病毒——比如你在大流行中遇到的那种——在你的鼻子或喉咙里安家。
杰克逊说,这些实验中使用的物质可能被优化用于呼吸道病毒暴露后不久的鼻腔喷雾剂,或作为预防药物。
他说:“用局部应用的短时药物延迟病毒的进入、退出或传播,将有助于我们的免疫系统赶上并及时到达,阻止全面感染,并有望限制未来的大流行。”
更多信息:吴建廷等,SARS-CoV-2在气道上皮细胞中的复制需要运动纤毛和微绒毛重编程,细胞(2022)。DOI: 10.1016 / j.cell.2022.11.030