科学家在破解失眠基因方面取得进展
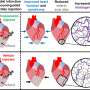
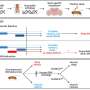
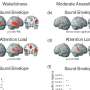
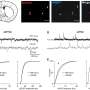
![Translating human GWAS signals to functional outcomes with variant-to-gene mapping. (A) Leveraging existing insomnia human GWAS loci, we identified proxy SNPs in strong linkage disequilibrium with sentinel SNPs using both genome-wide ATAC-seq and high-resolution promoter-focused Capture C data from iPSC-derived NPCs and then performed high-throughput sleep and activity screening using Drosophila RNAi lines with confirmation in a vertebrate zebrafish (Danio rerio) model. (B to D) Three examples of chromatin loops linking insomnia associate SNPs to candidate effector genes in NPCs. (B) rs13033745 [coefficient of determination (r 2 ) with sentinel SNP rs1519102 = 0.84] loops to the MEIS1 promoter region. (C) rs9914123 (r 2 with sentinel SNP rs11650304 = 0.76) loops to the promoters of SP2, PRR15L, CDK5RAP3, NFE2L1, CBX1, and HOXB3 in a ~700-kb region. (D) rs3752495, rs8062685, and rs9932282 (r 2 with sentinel SNP rs3184470 = ~1) loop to the promoters of PIG-Q, NHLRC4, and NME4. Orange box, sentinel SNP. Black bars, open chromatin peaks from ATAC-seq. Magenta arcs, chromatin loops from promoter-focused Capture C. Neuronal enhancer and promoter tracks are from. Credit: Science Advances (2023). DOI: 10.1126/sciadv.abq0844 科学家在破解失眠基因方面取得进展](https://scx1.b-cdn.net/csz/news/800a/2023/scientists-make-progre.jpg)
德克萨斯农工大学、宾夕法尼亚大学佩雷尔曼医学院和费城儿童医院(CHOP)的研究人员共同开展了一项研究,利用人类基因组学确定了从果蝇到人类睡眠调节的一种新的遗传途径,这一新颖的见解可能为失眠和其他与睡眠有关的疾病的新疗法铺平道路。
德克萨斯农工大学的遗传学家和进化生物学家亚历克斯·基恩与宾夕法尼亚大学的艾伦·帕克、菲利普·格尔曼以及CHOP的斯特鲁恩·格兰特合作进行了这项开创性的研究,该研究发表在《科学》杂志上科学的进步.
“通过人类基因组研究来寻找睡眠已经付出了巨大的努力基因基恩说。“一些研究涉及了数十万人。但在动物模型中的验证和测试对于理解功能至关重要。我们在这里取得了这一成就,很大程度上是因为我们每个人都带来了不同领域的专业知识,使这次合作获得了最终的效果。”
基恩说,该团队工作中最令人兴奋的事情是,他们开发了一个管道,而不是从一个开始生物模型,但有实际的人类基因组数据。
基恩说:“有大量的人类全基因组关联研究(GWAS)确定了与人类睡眠相关的遗传变异。”“然而,验证它们一直是一个巨大的挑战。我们的团队使用了一种称为变体到基因图谱的基因组学方法来预测受每种遗传变异影响的基因。然后我们筛选了这些基因在果蝇.
“我们的研究发现,蛋白质功能调节剂的生物合成所必需的Pig-Q基因突变可以增加睡眠。然后我们在脊椎动物模型斑马鱼上进行了测试,发现了类似的效果。因此,在人类、苍蝇和斑马鱼中,Pig-Q与睡眠调节有关。”
基恩说,研究小组的下一步是研究一种常见的蛋白质修饰——gpi锚生物合成——在睡眠调节中的作用。此外,他指出,该团队开发的人类-果蝇-斑马鱼管道不仅可以在功能上评估睡眠基因,还可以在功能上评估使用人类GWAS研究的其他特征,包括神经退行性变、衰老和记忆。
宾夕法尼亚大学精神病学临床心理学副教授格尔曼说:“了解基因如何调节睡眠以及这一途径在睡眠调节中的作用,可以帮助解开未来关于睡眠和睡眠障碍(如失眠)的发现。临床心理学家宾夕法尼亚大学时间生物学和睡眠研究所。“展望未来,我们将继续使用和研究这个系统,以确定更多调节睡眠的基因,这可能为治疗睡眠障碍的新方法指明方向。”
基恩在他的生物钟研究中心附属实验室的研究处于进化和神经科学的交叉点,主要集中在理解睡眠的神经机制和进化基础,记忆形成和其他行为功能在苍蝇和鱼模型中。具体来说,他研究了果蝇(Drosophila melanogaster)和墨西哥洞穴鱼,它们都失去了视力和语言能力睡眠目的是找出行为选择的遗传基础哪些因素人类疾病包括肥胖、糖尿病和心脏病。
更多信息:Justin Palermo等人,变异到基因定位,然后跨物种遗传筛选,确定gpi锚生物合成为新的睡眠调节器,科学的进步(2023)。DOI: 10.1126 / sciadv.abq0844.www.science.org/doi/10.1126/sciadv.abq0844