三阴性乳腺癌的新治疗靶点发现
针对细胞post-transcription机制CD73胞外酶可以促进抗肿瘤免疫和三阴性乳腺癌癌症进展缓慢,根据西北医学研究发表在科学的进步。
共同领导的这项研究本章,医学博士,博士,教授,医学分部的血液学和肿瘤学和Microbiology-Immunology,表明新患者的免疫治疗策略目前缺乏有效的治疗方法。
”三阴性乳腺癌,你要考虑针对主要的免疫抑制机制,并针对CD73现在已经成为一个新兴的选择除了其他传统检查点封锁,”张先生说,他也是肿瘤的领头人,环境&转移(团队)计划在西北大学的罗伯特·h·劳瑞综合癌症研究中心。
三阴乳腺癌(TNBC)细胞一般不包含典型的激素和受体蛋白中发现乳腺癌细胞,数量有限的可行的治疗靶点。
除了手术,放疗和化疗,免疫疗法等免疫抑制剂检查站药物,识别并阻止特定蛋白或“检查点”产生的免疫细胞和癌症细胞被广泛用于治疗实体肿瘤,包括TNBC。然而,之前的临床试验表明,大多数TNBC患者几乎没有应对这种疗法。
在当前的研究中,研究人员旨在确定新的治疗靶点,可以调动人体的免疫系统来克服肿瘤导致的免疫抑制TNBC细胞。
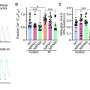
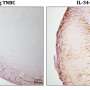
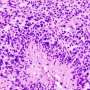
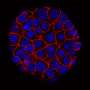
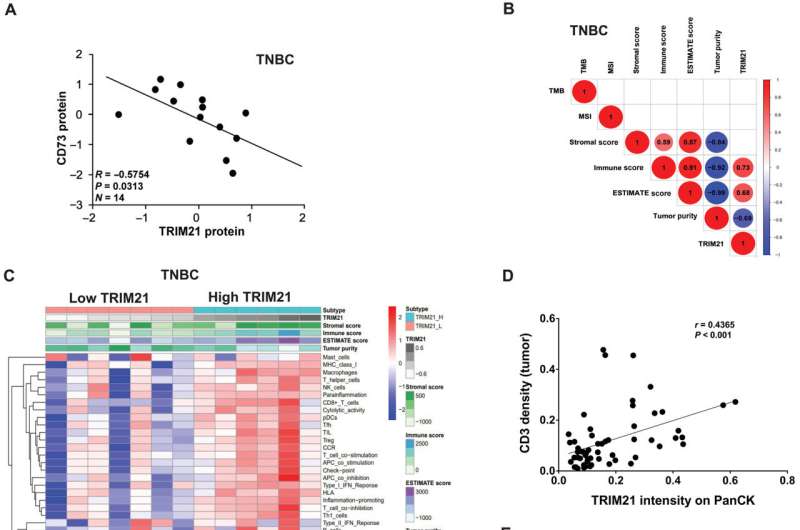
通过分析TNBC细胞株,研究团队发现高浓度的活性胞外酶CD73表达在肿瘤细胞的表面。增加表达CD73异常,根据张,这表明高浓度的酶增加肿瘤微环境中的免疫抑制活性。
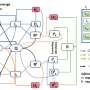
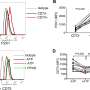
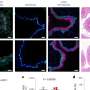
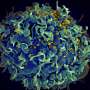
使用先进的显微镜技术进一步探讨癌细胞,调查人员发现ubiquitinase蛋白质TRIM21介导CD73的退化,并扰乱TRIM21稳定CD73,反过来,抑制cd8 + t细胞,否则他们就会提升对癌症的适应性免疫反应。
“因此,你可以提供额外的选项来生成试剂块结构这两个分子之间的相互作用,”张说。
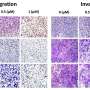
研究者也从CD73提取特定的氨基酸,CD73的基本细胞功能退化,特别是ubiquitylation,防止抗肿瘤免疫力和增强肿瘤的生长。
总的来说,研究结果揭示了一个新的潜在的治疗策略,减轻CD73蛋白质含量可以防止TNBC肿瘤进展。
CD73水平降低,增加TRIM21水平癌症细胞也可以作为生物标志物识别患者免疫治疗可能更有利的反应,根据张。
“我们认为如果你直接调节CD73蛋白水平,不仅可以降低酶活性也可以针对CD73独立的酶活性功能”,张说。
更多信息:章子怡傅et al,蛋白水解调节CD73 TRIM21协调肿瘤免疫原性,科学的进步(2023)。DOI: 10.1126 / sciadv.add6626。www.science.org/doi/10.1126/sciadv.add6626