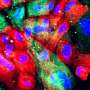
身体的防御系统是如何控制武器的
免疫系统的信号分子只在必要时才会触发反应。为了防止危及生命的扩散到身体其他部位,结缔组织可以像海绵一样吸收这些分子。托马斯·布兰肯斯坦领导的团队在自然免疫学.
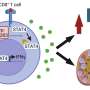
当T细胞免疫系统它们在细胞因子的帮助下进行交流。细胞因子家族的一个重要成员是干扰素- γ,这是一种激活身体防御的蛋白质,特别是在对抗病毒和细菌时。
在进化的过程中,人体已经发展出各种各样的策略来防止免疫反应过度。柏林Max Delbrück中心分子免疫学和基因治疗实验室主任托马斯·布兰肯斯坦教授领导的德法研究小组现在发现了另一种重要的机制。
这一切都取决于四个氨基酸
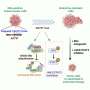
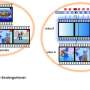
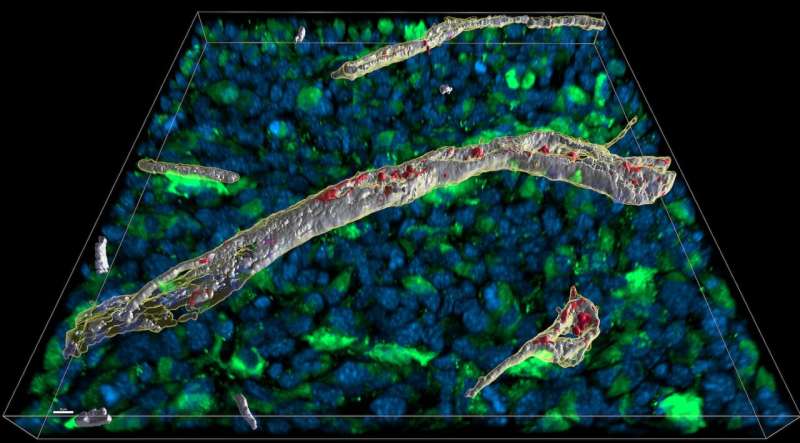
在杂志上发表的一篇论文中自然免疫学,科学家解释了干扰素是如何利用四种氨基酸与细胞外基质结合的结缔组织,形成了一个网络之间单个细胞从而调节细胞间的接触。该研究的第一作者Josephine Kemna博士解释说,这种结合可以防止细胞因子在全身扩散并引发危险的免疫反应。
她说,当结合所需的氨基酸缺乏时,结果是身体的防御能力严重受损。凯姆纳在2017年至2022年期间是布兰肯斯坦团队的成员。去年,她跳槽到柏林生物技术公司T-knife therapeutics——这是布兰肯斯坦实验室的一个分支。Kemna通过这项最新研究完成了她的博士学位,Charité-Universitätsmedizin柏林在其中也发挥了关键作用。这项研究得到了威廉·桑德基金会的资助。
这项研究的起点是Blankenstein和他的团队几年前的一项观察:“我们注意到细胞因子干扰素γ的分子结构在不同物种之间差异很大,”Thomas Kammertöns博士解释说,他是团队的另一名成员,也在Charité免疫学研究所工作。
他与布兰肯斯坦一起指导凯姆纳的博士论文,并被列为最后一位作者。然而,一个由四个氨基酸组成的短序列,即KRKR基序,在脊椎动物的整个进化过程中几乎没有变化。在我们研究的所有50个物种中,超过4.5亿年。”基于这一发现,研究小组推断KRKR基序在细胞因子的功能中起着重要作用,并决定验证这一假设。
在血液中迅速变成有毒物质
研究人员开始使用一种小鼠模型由Kammertöns开发,使他们能够调节产生的干扰素的浓度。Kammertöns解释说:“我们已经能够从这个模型中确定,γ干扰素很快就会变得有毒,血液中这种信号分子浓度高的动物几天内就会生病。”
生化分析还显示,一旦蛋白质通过带有四个正电荷的氨基酸的T细胞分泌出来,它就会与带负电荷的细胞外基质结合,即与分子硫酸肝素结合。
Kammertöns说:“这确保了干扰素γ被保留在局部,并防止它扩散到全身。”然而,鉴于硫酸肝素的结构因组织、细胞类型甚至细胞状态而异,结缔组织结合干扰素- γ的能力也可能不同,Université Grenoble-Alpes的Hugues Lortat-Jacob教授补充道,他也参与了这项研究。
下一步,该小组求助于Max Delbrück中心基因组编辑和疾病模型实验室的负责人Ralf Kühn博士,以帮助开发一种可以产生没有KRKR基序的干扰素分子的模型。为了做到这一点,Kühn和他的团队使用CRISPR-Cas9基因编辑技术从小鼠的细胞因子中去除了四种氨基酸。
“很长一段时间以来,科学家们一直认为信号分子依赖于这个结合位点来发挥作用,”Kammertöns说。“所以我们首先要证明事实并非如此。”该团队确实能够证明,即使没有KRKR基序,γ干扰素仍然附着在细胞表面的受体上,并在免疫反应中发挥其通常的作用。
高效的防御机制
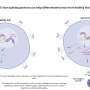
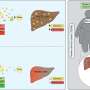
通常情况下,免疫系统会对抗病毒感染,并最终将其消灭。然而,对于γ干扰素中缺乏这四种氨基酸的小鼠来说,情况并非如此。Kammertöns报道说:“动物的免疫系统仍然能够调节对只引起非常短暂炎症反应的病毒的免疫反应。”在这些情况下,血液中干扰素- γ的含量最初确实增加了,但随后又迅速下降。
“然而,当小鼠感染了LCM病毒时,这种病毒会导致一种名为淋巴细胞性绒毛膜脑膜炎的流感样疾病,并使免疫系统在较长时间内忙碌,基因编辑的小鼠很快就会因为血液中高浓度的干扰素- γ而生病。”
“在我看来,从我们的研究中可以清楚地看出,我们的免疫系统已经发展出了强大的机制来控制自己的防御,”第一作者Kemna说。她说,如果这些机制不能正常工作,免疫系统最终可能会由于某些分子的毒性作用而破坏自身的机体,因为它们继续扩散。
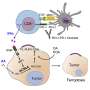
“我们发现的机制表明,进化确保了有毒分子通常只在需要它们的地方起作用,也就是说,在T细胞识别病毒感染细胞的地方。”
预防致命感染
“这项研究对免疫学和我们对人类许多炎症性疾病的理解具有重要意义人体Kammertöns说。他还解释说,细胞外基质在男性和女性中具有不同的结构,因此新发现的机制可以解释为什么一些传染性和自身免疫性疾病在男性和女性中进展如此不同。
Kammertöns补充说:“如果没有我们与法国同事Hugues Lortat-Jacob的出色合作,我们永远不会取得这些新发现,他研究细胞外基质超过30年,是该领域的世界领先专家之一。”
Kammertöns现在正与他的小组组长Blankenstein和弗莱堡大学医学中心的科学家们一起计划下一阶段的研究。他们将一起在一个新模型上测试他们的最新发现。Kammertöns说:“我们想要与所谓的野生老鼠一起工作,这些老鼠已经经历了几次感染,因此它们的免疫系统引发的反应更类似于人类。”
布兰肯斯坦总结道:“在进化的过程中,免疫系统在对抗病原体的军备竞赛中发展出了越来越强大的武器。”“我们的工作发现了一种新的机制,可以在不降低效率的情况下制衡这些武器库免疫反应——四氨基酸用干扰素γ防止传染病造成更多的死亡。”
因此,进一步了解干扰素- γ和细胞外基质之间相互作用的确切细节是有意义的。
更多信息:Josephine Kemna等人,IFNγ与细胞外基质结合可防止致命的全身毒性,自然免疫学(2023)。DOI: 10.1038 / s41590 - 023 - 01420 - 5