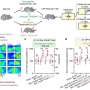
可卡因使用障碍改变了人类神经炎症和神经传递的基因网络
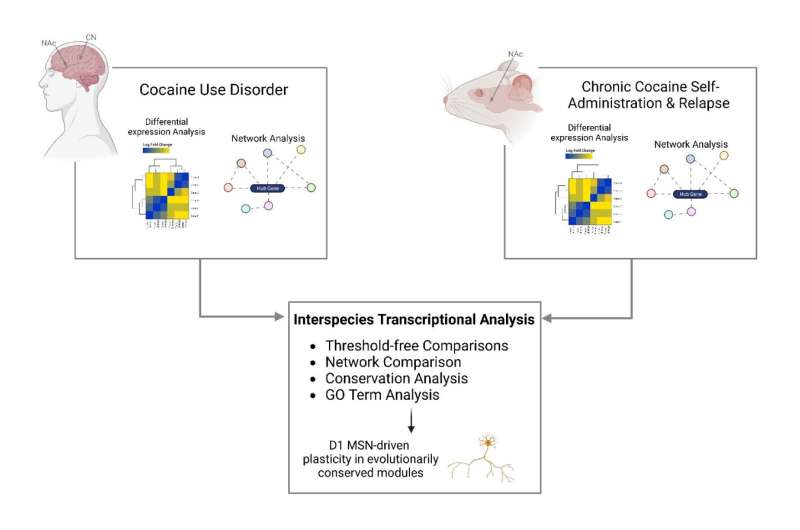
根据西奈山伊坎医学院进行的研究,可卡因使用障碍的个体在两个大脑区域表现出基因表达的变化:伏隔核,一个与奖励有关的区域,和尾状核,一个调节习惯形成的区域科学的进步。
这些变化导致了药物成瘾中出现的持续性行为异常,发生的原因是可卡因的使用引发一系列化学反应,导致这两个大脑区域中受影响基因产生的信使RNA数量增加,而其他基因的活性则下降。
信使RNA产生量的变化——这一过程也被称为潜在基因的“表达”——导致产生的蛋白质数量的变化以及随后执行的蛋白质数量的变化化学反应在大脑里。研究小组发现,这两种基因表达的rna之间存在显著的重叠大脑区域,这表明这些分子变化可能是糖尿病发展和维持的关键可卡因使用障碍。
可卡因使用障碍是一种慢性复发性脑部疾病,目前还没有fda批准的药物治疗方法。尽管假设大脑奖励和动机中心的基因表达调节在定义成瘾的持续行为变化中起着关键作用,但对于慢性可卡因使用在人类这些回路中引起的适应不良基因活动以及可卡因使用障碍的基础,我们的知识仍然有限。
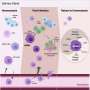
为了解决这一知识鸿沟,研究小组对两种基因进行了RNA测序伏隔核以及来自可卡因使用障碍患者和匹配对照者死后脑组织的尾状核。利用迄今为止最大和最多样化的队列研究,他们发现神经炎症过程被抑制,而突触跨膜转运蛋白和促离子性受体(控制如何抑制的蛋白质)神经细胞在可卡因使用障碍患者的纹状体中丰富了大脑中彼此之间的交流。
可卡因会增加突触上的神经递质多巴胺的数量,突触是两个脑细胞之间的连接处,电信号在这里被转化为化学信号。研究小组发现,通过这样做,可卡因会引发一系列事件,激活大脑中一种名为环AMP的化学信使,然后引发基因表达的变化。
“除了对可卡因使用所带来的分子变化的新见解外,我们还发现患有可卡因使用障碍的人会出现失调基因与精神分裂症有关重度抑郁症这表明这些疾病可能共享一些潜在的基因调节和神经回路系统,”Philipp Mews博士说,他是伊坎西奈山神经科学讲师,与神经科学博士生Ashley M. Cunningham一起撰写了这篇论文。
“重要的是,转录异常——特别是可卡因使用障碍患者伏隔核中被抑制的神经炎症反应——与阿片类药物使用障碍引起的促炎症级联反应方向相反。观察到两者都有明显的分子变化物质使用障碍这可能对开发针对可卡因使用障碍的有针对性的有效治疗方法很有价值。”
因为很难直接研究可卡因等药物是如何影响大脑的人类的大脑在美国,研究人员经常使用动物模型来研究它们的效果。然而,一个关键的问题是,他们从这些动物模型中学到的东西是否与使用可卡因的人类大脑中发生的事情相似。
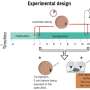
“我们的研究团队研究了在老鼠身上进行的研究,这些老鼠有机会自我服用可卡因,并比较了结果分子变化与可卡因使用障碍患者死后脑组织中所见的相比。我们的分析揭示了小鼠和人类大脑基因表达谱中惊人相似的变化,验证了使用小鼠模型来研究可卡因使用障碍的病理生理基础,”埃里克·j·内斯特勒医学博士说,他是纳什家族神经科学教授,弗里德曼大脑研究所主任,伊坎西奈山学术事务主任,西奈山卫生系统首席科学官,论文的高级作者。
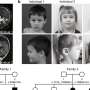
“同样重要的是要强调我们的人类大脑该队列包括大量黑人个体,他们在先前的可卡因使用障碍转录研究中没有得到很好的代表,尽管长期以来有证据表明,与可卡因有关的过量死亡率最高的是黑人个体。总之,这些发现代表着我们对可卡因使用障碍分子异常的理解取得了相当大的进步,并为未来的调查提供了极有价值的资源。”
更多信息:人类可卡因使用障碍和小鼠可卡因给药模型中纹状体基因网络的收敛异常科学的进步(2023)。