研究人员为Leigh综合征最常见的遗传原因开发了第一个有效的临床前模型

费城儿童医院(CHOP)的研究人员开发了两种新的斑马鱼模型,用于研究代表Leigh综合征最常见原因的线粒体疾病的特定遗传形式。利用这些模型,研究小组确定了两种已经被美国食品和药物管理局(FDA)批准用于其他疾病的药物,这些药物可以被重新用于治疗利综合征的这种特定原因。研究结果最近发表在该杂志上人类分子遗传学.
SURF1缺陷是Leigh综合征最常见的核遗传原因。SURF1基因对于将营养物质转化为细胞可利用的能量至关重要。SURF1基因中的致病突变破坏了线粒体呼吸链复合体IV的活动,阻止了能量的产生,并经常导致复合体医疗问题.
在受影响的患者中最常见的疾病类型是Leigh综合征,通常包括代谢性中风和癫痫发作、发育迟缓、周围神经病变,在某些情况下,还会导致儿童早期死亡。目前还没有fda批准的治疗Leigh综合征或任何由SURF1相关问题引起的疾病的疗法。
虽然其他几个临床前模型已经被用于研究SURF1疾病,许多这些尝试要么没有准确地复制疾病进展有经验的患者或不容易对研究潜在的治疗干预措施作出反应。为了解决这一问题,CHOP线粒体医学项目的研究人员使用CRISPR技术创建并表征了两种新型斑马鱼模型,这些模型更准确地代表了患有SURF1缺陷的患者遇到的临床问题。
“创建临床前模型,重现复杂罕见疾病的个体遗传原因的主要特征,对于使研究团队更好地理解健康问题的潜在机制,并发现多系统疾病的不同方面的潜在有效治疗方法至关重要,如利综合征,它可能通过各种挑战生命的症状对患者产生负面影响。”儿科教授、CHOP线粒体医学项目执行主任、该研究的高级合著者Marnbob电竞i Falk医学博士说。
“我们已经取得了巨大的成功,应用最新的遗传技术来建立和表征各种线粒体疾病的斑马鱼临床前模型,这项最新的研究证明了疾病特异性模型对我们确定目前治疗选择有限的主要疾病亚群患者的潜在治疗方法是多么重要。”
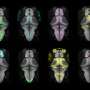
研究人员发现,随着缺乏surf1基因的斑马鱼年龄的增长,它们的眼睛出现了结构性问题,游泳活动减少,后者是能量水平下降的标志,也是线粒体疾病的一个标志性特征。这些斑马鱼幼虫还表现出急性应激敏感性,这是利综合征的另一个关键标志,可导致代谢性中风导致发育退化和神经退化。
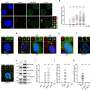
然而,当这些斑马鱼用半胱胺重酒石酸盐或n -乙酰半胱氨酸处理时,它们的氧化应激防御得到了改善,研究人员通过测量谷胱甘肽水平的增加来评估,谷胱甘肽是一种参与组织修复的物质。此外,这些治疗使斑马鱼更能抵抗应激源引起的脑死亡、游泳和神经肌肉功能障碍以及心跳丧失。
CHOP线粒体医学项目的研究助理教授、该研究的共同第一作者Suraiya Haroon博士说:“这些研究表明,这种治疗类型的治疗可能对预防SURF1患者的神经功能失代偿或潜在的其他遗传形式的Leigh综合征患者具有潜在的益处。”
一项针对包括SURF1疾病在内的所有已知Leigh综合征病因的国际多地点自然史研究目前正在进行中,以更好地衡量某些结果,这些结果可能用于未来治疗试验中的新疗法研究。
Falk说:“需要严格的临床试验来客观地确定这些药物是否可以预防Leigh综合征谱系障碍线粒体疾病患者的神经发育失代偿和/或改善神经结局。”
“然而,这些转化研究结果代表了我们对氧化应激在这种特殊形式的线粒体疾病中的重要性的理解的重要飞跃,并提供了客观证据,增强氧化应激防御可能会产生有意义的临床益处。”
更多信息:Suraiya Haroon等人,n -乙酰半胱氨酸和重酒石酸半胱胺通过恢复两种新型的Leigh综合征的surf1 - / -斑马鱼缺失模型中的谷胱甘肽平衡来预防叠氮类药物诱导的神经肌肉失代偿,人类分子遗传学(2023)。DOI: 10.1093 /物流/ ddad031