研究阐明了诱导癌细胞死亡的治疗策略

癌症是由基因突变引起的疾病。这些突变基因在癌症中分为两大类:肿瘤抑制基因和癌基因。肿瘤抑制基因的突变可以让肿瘤不受控制地生长——没有刹车的情况下——而致癌基因的突变可以激活细胞增殖,把油门一直踩到底部。
研究人员研究肿瘤抑制基因已经对p53和最常突变的肿瘤抑制基因在人类癌症。在过去的20年里,很多人致力于设计特异性激活p53的生物靶向疗法。
然而,虽然研究表明这些疗法在诱导p53活性方面是有效的,但它们通常不会致死癌症细胞。正如观察到的其他生物靶向治疗,p53的激活已被证明是停止的肿瘤的生长在一段时间内,但细胞最终会变异并对治疗产生抗药性。
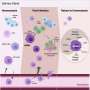
一项新的研究科罗拉多大学癌症中心的科学家阐明了防止p53激活引发有效癌细胞死亡的工作机制。他们表明,抑制两种不同的p53抑制因子可以通过激活互补基因网络(称为综合应激反应)引起癌细胞死亡。
“当你同时阻断p53的主要阻遏物MDM2和次要阻遏物PPM1D时,p53在诱导癌细胞死亡方面表现得更好,这种增强的杀伤活性需要综合应激反应”Joaquin Espinosa博士解释道,他是CU医学院的药理学教授,Linda Crnic唐氏综合症研究所的主任,也是该研究的高级作者。“这是使基于p53的生物靶向治疗更有效的重要一步。”
诱导癌细胞死亡
这一进展是哥伦比亚大学医学院药理学助理研究教授Zdenek Andrysik博士和埃斯皮诺萨实验室其他成员近二十年研究的一个重要里程碑。他们和其他的研究致力于了解MDM2和PPM1D的作用,这两种蛋白质在肿瘤细胞内抑制p53,以及抑制它们导致癌细胞死亡的机制。
埃斯皮诺萨解释说:“已经确定MDM2是一个主要的抑制因子,PPM1D是一个次要的抑制因子。”很长一段时间以来,人们都希望只抑制主要的抑制因子就足够了。在发展方面投入了大量精力小分子为了阻断MDM2,花费了数百万美元,但这些药物在临床试验中表现不佳。”
研究人员随后转向轻微的抑制因子,包括PPM1D。“我们对PPM1D和p53的其他轻微抑制因子知之甚少,”Andrysik说,“但很快就清楚了,如果同时抑制MDM2和PPM1D, p53可以有效地诱导癌细胞死亡。然而,推动这种协同作用的潜在机制尚不清楚。”
了解机制
Espinosa和Andrysik已经能够证明抑制MDM2和PPM1D激活综合应激反应,这是一种刺激ATF4蛋白质的信号通路。他们进一步证明,ATF4与p53合作,共同导致癌细胞死亡。
Andrysik说,抑制MDM2和PPM1D,从而允许p53与ATF4合作杀死癌细胞,在实验室中对多种癌症类型显示出了希望。这一机制洞察很快揭示了诱导癌细胞死亡的其他药理学策略。
例如,Andrysik和Espinosa改变了药物奈非那韦的用途,奈非那韦最初被批准用于治疗艾滋病毒。埃斯皮诺萨说:“现在我们知道奈非那韦激活了综合应激反应,因此成为了与MDM2抑制剂的一个很好的组合。”
Andrysik和Espinosa正在继续他们的研究,以更多地了解当MDM2和PPM1D被抑制而p53被激活时发生的协同反应机制。Andrysik说:“我们的数据表明,癌细胞特别容易受到p53和综合应激反应的双重激活,这可能为临床提供了一个治疗窗口,使正常细胞免受p53的杀伤作用。”
埃斯皮诺萨补充说:“癌症研究的圣杯一直是恢复p53活性以诱导肿瘤消退。在过去的二三十年里,很多研究都致力于寻找更优雅的方案来解决广泛作用的化疗或放疗。随着我们对癌症中突变的基因和蛋白质了解得更多,我们更能看到什么时候刹车失灵并将其恢复,或者当油门踏板一直踩到地板时,用特定的靶向抑制剂将其抬起。”
更多信息:Zdenek Andrysik等人,PPM1D通过抑制综合应激反应抑制p53依赖的转激活和细胞死亡,自然通讯(2022)。DOI: 10.1038 / s41467 - 022 - 35089 - 5