研究揭示了CBD如何对抗癫痫发作
一项研究揭示了一种以前不为人知的方式,大麻中发现的一种物质大麻二酚(CBD)可以减少许多治疗耐药形式的儿童癫痫发作。
由纽约大学格罗斯曼医学院的研究人员领导的这项新研究发现,CBD阻断了一种名为溶血磷脂酰肌醇(LPI)的分子所携带的信号。中发现的大脑细胞被称为神经元的LPI被认为是放大的神经信号作为正常功能的一部分,但可能被疾病劫持,导致癫痫发作。
在线发布于2月13日神经元这项研究证实了之前的发现,即CBD会阻碍LPI放大大脑海马区神经信号的能力。目前的研究结果首次表明,LPI也削弱了对抗癫痫的信号,进一步解释了CBD治疗的价值。
“我们的研究结果加深了该领域对中枢癫痫诱发机制的理解,对寻求新的治疗方法具有许多意义,”纽约大学朗格尼健康中心生理学和神经科学系主任、通讯作者理查德·w·钱说。
Tsien补充说:“这项研究不仅阐明了CBD是如何对抗癫痫发作的,而且更广泛地阐明了大脑回路是如何平衡的。”“相关的失衡在自闭症和精神分裂症中也存在,所以这篇论文可能会产生更广泛的影响。”
致病循环
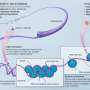
研究结果建立在每个神经元如何“激发”向自身延伸发送电脉冲,直到它到达突触,突触是连接神经元通路中的下一个细胞的间隙。当脉冲在突触之前到达细胞的末端时,它会触发一种叫做神经递质的化合物的释放,这种化合物漂浮在间隙中,影响下一个细胞。在交叉时,这样的信号要么鼓励细胞放电(兴奋),要么对放电施加刹车(抑制)。两者之间的平衡对大脑功能至关重要;过度兴奋会诱发癫痫。
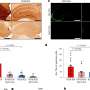
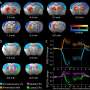
这项新研究观察了几种啮齿动物模型,以探索癫痫发作背后的机制,通常是通过用细尖端电极测量携带信息的电流流动。其他实验通过基因上去除LPI的主要信号伙伴,或通过测量癫痫发作后LPI的释放来观察LPI的影响。
这些测试证实了过去的发现,LPI通过与神经元细胞表面的一种叫做g偶联受体55 (GPR55)的蛋白质结合来影响神经信号。这种LPI-GPR55突触前相互作用被发现会导致细胞内钙离子的释放,从而鼓励细胞释放谷氨酸盐,这是主要的兴奋性神经递质。此外,当LPI激活突触另一侧的GPR55时,它通过减少抑制所必需的蛋白质的供应和适当的排列来削弱抑制。作者说,总的来说,这创造了一个“危险的”双管齐下的机制来增加兴奋性。
研究小组发现,要么对小鼠进行基因工程,使其缺乏GPR55,要么在诱发癫痫的刺激之前用植物来源的CBD治疗小鼠,都阻止了lpi介导的兴奋性和抑制性突触传递的影响。而之前的研究表明GPR55是一种癫痫发作目前的工作提供了更详细的、建议的作用机制。
作者提出,CBD阻断了一个“正反馈循环”,在这个循环中,癫痫发作会增加LPI-GPR55信号,这可能会鼓励更多的癫痫发作,从而增加LPI和GPR55的水平。提出的恶性循环提供了一个可以解释重复的过程癫痫发作,尽管还需要进一步的研究来证实这一点。
此外,目前的研究检测了基于植物的大麻素CBD,但作者指出,LPI是信号网络的一部分,其中包括“内源性大麻素”,如2-花生四烯酰甘油(2-AG),它们自然存在于人类组织中。LPI和2-AG靶受体也受CBD调控,但在突触上的作用不同。当LPI放大传入的电信号时,像2-AG这样的内源性大麻素会对脑电信号的增加做出反应大脑的活动通过减少神经细胞释放的神经递质。有趣的是,LPI和2-AG可以通过酶的作用相互转化。
“从理论上讲,大脑可以通过在促兴奋性LPI和2-AG的恢复作用之间切换来控制活动,”该研究的第一作者埃文·罗森伯格博士说,他是Tsein实验室的博士后学者。“药物设计者可以抑制支撑LPI产生的酶或促进其转化为2-AG,作为控制癫痫发作的另一种方法。LPI也可以作为一种生物标志物癫痫发作或预测对CBD的临床反应,为未来的研究提供了一个领域。”
更多信息:Richard Tsien和同事,大麻二酚通过调节兴奋-抑制比率来对抗海马过度活跃,神经元(2023)。DOI: 10.1016 / j.neuron.2023.01.018.www.cell.com/neuron/fulltext/s0896 - 6273 (23) 00066 - 1