科学家在肺癌研究中发现了关键的“罪魁祸首”
在英国,肺癌是癌症死亡的最大原因,但南安普顿大学的一组科学家的一项研究发现了一种新方法,可以识别出死于这种疾病的患者是死于这种疾病的两倍。
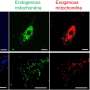
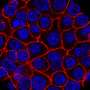
来自大学癌症免疫学中心的研究人员使用最先进的技术来了解肿瘤周围的一种特殊类型的细胞,称为癌细胞纤维母细胞-比以往任何时候都更详细。这些都是健康的细胞它们支持伤口愈合,但可能会被癌症劫持,帮助肿瘤生长和扩散。
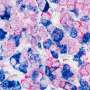
利用大学工程师发明的设备和最新的技术,他们首次能够识别出三种不同类型的成纤维细胞——一种“被劫持的”肌成纤维细胞和两种“正常的”成纤维细胞。
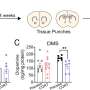
研究表明,肌肉成纤维细胞比例高的患者死于这种疾病的风险增加了一倍肺癌与肿瘤中肌成纤维细胞较少的患者相比。这一发现发表在该杂志上自然通讯.
联合领导这项研究的克里斯·汉利博士说:“这些类型的成纤维细胞表明患者是否能存活更长或更短的时间,所以这一信息可能会被用来给他们一个更准确的预后。
“我们还相信,肿瘤中有大量肌成纤维细胞的患者可以从针对这种特定细胞的新治疗中受益,最终提高生存率。”
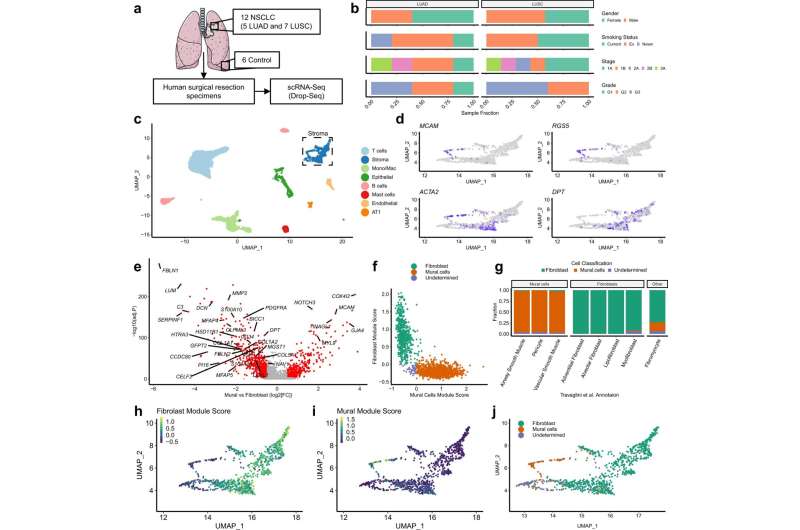
研究小组分析了来自100名患者的1万个成纤维细胞,使用单细胞测序技术逐个分解它们。
利用南安普顿大学工程师制造的机器,科学家们能够捕捉到个体细胞在细胞破裂以捕获不同的分子之前,变成一个液滴。这使他们能够计算出给定细胞中有多少不同的分子,从而为其提供指纹。
这项技术揭示了三种类型的成纤维细胞,每一种都有自己的分子指纹和功能。这些指纹被用来追踪成纤维细胞的来源,并表明只有肌成纤维细胞与增加死于肺癌的风险直接相关。
克里斯·汉利博士说:“到目前为止,还不清楚是否所有的成纤维细胞都对癌症有帮助,但这项研究表明,肌成纤维细胞是最危险的罪魁祸首。如果我们能去除肌成纤维细胞,我们就有更好的机会去除肺癌。”
这是迄今为止对肺癌患者成纤维细胞进行的最大规模的研究,耗时6年完成。这是克里斯·汉利博士和加雷斯·托马斯教授早在技术的进步是为了让他们进行研究。
联合负责人托马斯教授说:“当这是一项非常新的技术时,我们就开始了这个想法,我们经历了漫长的过程,做了大量的工作才能达到这一点。但它给我们的洞察力为未来的项目提供了很多机会,因此我们对我们的方向有了更清晰的想法。
“下一步是开发针对‘坏’成纤维细胞的方法,使治疗对高危肺癌患者更有效。”
英国癌症研究中心研究与创新执行主任Iain Foulkes博士说:“为了更快地战胜癌症,我们需要详细地了解它。多亏了这样的开创性研究,我们离所有患者都能接受根据其肿瘤特征量身定制的治疗的那一天越来越近了。
“今天癌症研究人员可用的技术让我们对癌症的发生和发展有了前所未有的了解。我们希望这项研究将成为新的治疗方法的基础癌症在将来的诊所里。”
更多信息:Christopher J. Hanley等人,单细胞分析揭示预后成纤维细胞亚群与肺癌分子和免疫亚型相关,自然通讯(2023)。DOI: 10.1038 / s41467 - 023 - 35832 - 6