天使综合征患者的治疗窗口可能比以前报道的更宽
天使综合征是一种罕见的神经发育障碍,其特征是大脑结构变化、严重的智力残疾、语言障碍、运动功能障碍、癫痫、睡眠和独特的行为,每10,000到24,000人中就有一人患有这种疾病,目前还没有治愈或治疗方法。
德克萨斯儿童医院和贝勒医学院的Jan and Dan Duncan神经学研究所(Duncan NRI)的研究人员现在发现,一种基因治疗方法可以有效逆转成年和幼年啮齿动物模型中这种疾病的关键症状,这表明Angelman综合征的治疗年龄窗口比以前报道的要宽得多,并为受这种毁灭性疾病影响的患者及其家庭带来了新的希望。
此外,该研究还揭示了两个临床重要的生物标志物,可用于评估这种治疗方法和其他治疗方法在未来临床试验中对这种疾病的疗效。这项研究最近发表在eLife.
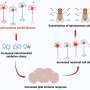
天使综合征是由父系Ube3a基因拷贝失活引起的
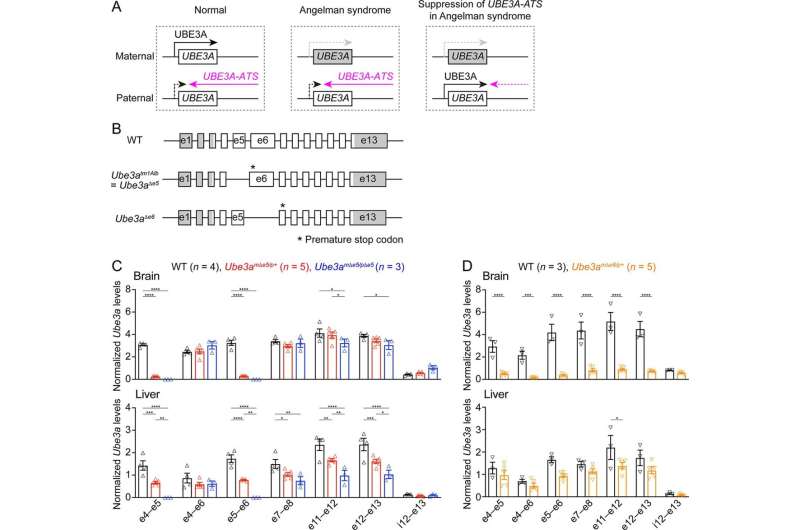
当母体遗传的UBE3A基因拷贝缺失或缺陷时,就会出现天使综合征。人们通常会从父母双方各继承一份UBE3A基因。在大多数组织中,该基因的两个拷贝都是激活的。然而,在中枢神经系统(即大脑和脊髓)的神经细胞中,这种表达基因复制收到的父亲是关闭(沉默)。这种现象的父母特异性激活和沉默基因被称为基因组印迹,因此,后代的神经元只有一个活跃的该基因副本。
如果这个活跃的母本拷贝由于染色体重排而丢失,或者由于突变而出现缺陷,就会导致神经元中UBE3A蛋白的完全丢失。这影响大脑发育和功能的各个方面,因为这种蛋白质对维持其他几种蛋白质的合成和降解之间的平衡至关重要。
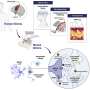
以前在安吉尔曼啮齿动物模型中的研究为这种遗传疾病的机制提供了一些见解,并确定了潜在的治疗策略。一种治疗策略可以解决这种遗传疾病的根本原因,并具有很大的前景,即使用反义寡核苷酸(ASOs)或CRISPR/Cas9等基因治疗方法重新激活UBE3A基因沉默的父拷贝。
值得注意的是,先前的概念验证研究表明,如果在非常年轻的年龄进行治疗,这种方法可以有效地恢复天使综合征动物模型中的一些神经症状。
“之前使用ASO策略的研究能够挽救一些人神经系统症状在年轻的动物中,但这种方法在年老的动物中效果较差。这些实验表明,为了获得最大的效益,理想情况下,这种方法必须非常早地使用,甚至可能在天使患者的子宫内使用,”贝勒学院助理教授、邓肯NRI研究员薛明善博士说。
这引起了人们对其有效性的担忧人体临床试验因为典型的天使患者在1到4岁之间被诊断出患有这种疾病。因此,我们决定测试给老年安琪尔曼小鼠服用ASO是否会改善两种症状——大脑异常电活动和睡眠障碍——这两种症状在临床上都非常重要,但尚未在这种治疗的背景下进行研究。”
使用新生成的Angelman小鼠模型识别生物标志物,用于后期干预
在这项研究中,Xue和他的团队首先生成了一个新的天使人综合征的空鼠模型。与现有的Angelman综合征模型不同,在这个新的小鼠模型中,Ube3a mRNA和蛋白质的水平都降低了,他们假设这将有助于更好、更精确地评估通过ASOs的基因治疗。
他们使用这种新的小鼠模型来检验基因疗法在幼年和成年Angelman综合征小鼠模型中是否能逆转三种强有力的临床关键症状——大脑神经元的过度兴奋性(与癫痫有关),大脑异常的电活动(与认知表现有关),以及睡眠障碍——这些症状以前从未被测试过。
这些症状与疾病进展和/或严重程度密切相关,如果这种治疗有效,作者预测它们可以作为生物标志物,指导治疗开发和未来更广泛患者的临床监测。
基因治疗改善异常脑电图模式和睡眠障碍在新的啮齿动物模型
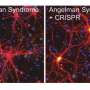
他们发现,将ASO直接注射到新生成的Angelman疾病模型的大脑中,会导致整个大脑中Ube3a父本拷贝的长期重新激活,以及Ube3a蛋白的上调,这一上调持续了至少10周。
正如预期的那样,他们生成的新的Ube3a动物模型也表现出异常的大脑活动和睡眠障碍,这两者都被ASO注射和伴随的父Ube3a基因的重新激活所逆转,尽管这不足以观察到神经元过度兴奋性的任何变化。
“我们的研究对未来使用这种方法进行的临床试验以及其他针对安吉尔曼综合征的临床试验有几个意义,”薛博士说,他也是戈登和玛丽·凯恩儿童神经学研究基金会实验室和卡罗琳·德卢卡学者的研究员。
“首先,我们的研究结果表明,不同年龄段的天使综合征患者可能受益于这种基因治疗。其次,Ube3a水平与脑电图功率谱之间的强大相关性支持了这一指标可以作为未来临床试验中这种疾病的定量生物标志物的概念。第三,由于脑电图功率与症状严重程度密切相关,包括患者的认知行为,因此有理由推测这种基因治疗方法也可能改善天使综合征患者的认知功能。”
“最后,临床医生和护理人员一致报告睡眠障碍是最具挑战性的症状之一,也是新疗法发展的重要考虑因素。我们的基因治疗方法在天使综合症小鼠模型中证明了睡眠障碍的减少,如果这一发现在人体试验中也成立,我们希望这种基因治疗方法能显著改善天使综合症患者、他们的照护者和家庭成员的生活质量。”
更多信息:Dongwon Lee等人,反义寡核苷酸疗法拯救天使综合征青少年和成年小鼠模型中受干扰的脑节律和睡眠,eLife(2023)。DOI: 10.7554 / eLife.81892