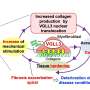
整合结构生物学为囊性纤维化治疗提供了新的线索
圣裘德儿童研究医院和洛克菲勒大学的科学家们结合他们的专业知识,更好地了解囊性纤维化跨膜电导调节因子(CFTR)。CFTR基因突变会导致囊性纤维化,这是一种无法治愈的致命疾病。
目前使用一种称为增强剂的药物的治疗可以增强一些患者的CFTR功能;但是电位器是如何工作的还不是很清楚。新的发现揭示了CFTR如何机械地发挥作用,以及疾病突变和增强因子如何影响这些功能。有了这些信息,研究人员可能能够设计出更有效的囊性纤维化治疗方法。这项研究今天发表在自然.
囊性纤维化是一种遗传疾病,会导致人们产生过于粘稠的粘液。这会阻塞气道,导致肺损伤,并引起消化问题。这种疾病影响着美国大约3.5万人。CFTR是一种阴离子通道,是一种通过上皮和其他膜维持盐和液体正确平衡的通道。CFTR的突变是导致囊性纤维化的原因,但这些突变可以以不同的方式影响CFTR功能。因此,一些用于治疗该病的药物只能部分恢复CFTR特定突变形式的功能。
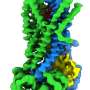
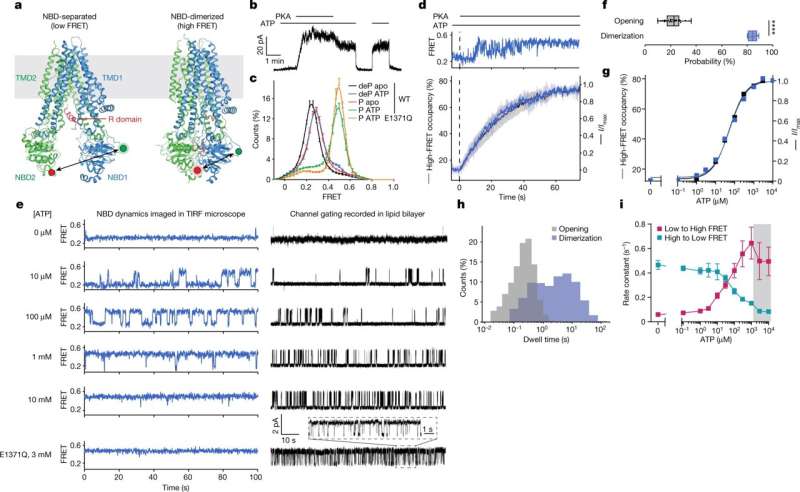
CFTR的结构,先前在洛克菲勒大学的Jue Chen博士及其同事的实验室中捕获,揭示了两种不同的构象(形状)。这些静态图像使研究人员能够看到通道在打开或关闭时的状态,但状态之间的转换还不完全清楚。
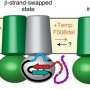
因此,构象变化对通道的打开和关闭是重要的,解释了CFTR的电生理特性,这已经被分析了几十年。这些发现激发了人们对直接实时可视化CFTR结构转变和检查构象变化如何受到影响的兴趣疾病的突变以及用于增强患者CFTR功能的药物。
“通过这次合作,我们有机会真正深入研究结构和功能之间的关系,”圣裘德结构生物系的共同通讯作者斯科特·布兰查德博士说。“我们实验室之前对核糖体和g蛋白偶联受体的研究表明,这是可能的,但很少单一的蛋白质与CFTR相比,这与疾病的治疗更相关,因为囊性纤维化的治疗旨在改善这种蛋白质突变形式的缺陷。
“进行生物物理测量并获得这些类型的定量见解的能力是单分子成像的进步之一,它从未停止让我感到惊讶。”
合作带来突破
研究小组的互补专业知识是取得发现的关键。通过电生理学和结构研究,洛克菲勒团队能够指导圣裘德团队放置单分子探针。通过部署单分子荧光共振能量转移(smFRET), St. Jude团队能够为CFTR机械的运动部件提供新的见解。
通过低温集成电子显微镜该研究小组能够更好地理解CFTR工作原理所需的联系。
“通过了解CFTR的结构和行为,这有可能帮助囊性纤维化患者,”洛克菲勒大学的第一作者Jesper Levring说。“使用这些方法——单通道电生理学和smfret——一次一个地观察这些分子,我们可以将通道的功能与脑电信号联系起来构象变化并将其与潜在的结构生物学联系起来。”
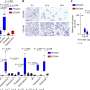
研究人员发现,CFTR呈现出一种等级森严的门控机制。CFTR的两个核苷酸结合域在通道打开之前二聚(结合)。二聚通道内的构象变化,与ATP水解(一种释放能量的反应)有关,调节氯化物电导。
这一机制见解的重要性通过发现增强剂药物Ivacaftor和GLPG1837在核苷酸结合域二聚化时通过增加孔开放来增强通道活性而得到进一步揭示。突变会导致囊性纤维化会降低二聚的效率。这些见解将有助于寻找更有效的临床治疗方法。
“这项工作最令人满意的是,我们回答了一个关于CFTR如何工作的问题,这个问题在该领域一直是争论多年的话题,”该研究的共同通讯作者陈说。
“每一种方法都有局限性,所以你可以有很好的数据,但仍然没有答案。通过结合方法,我们已经得到了一个统一的机制,让我们深入了解这种分子是如何工作的。有了这样的理解,我们就可以测试突变或药物是如何影响功能的,这就是我们最终如何获得更好的治疗方法。”
更多信息:陈珏,单分子分辨率下CFTR功能、病理和药理,自然(2023)。DOI: 10.1038 / s41586 - 023 - 05854 - 7.www.nature.com/articles/s41586 - 023 - 05854 - 7