是什么让血液干细胞转换?监管RNA拼接的可能答案
隆德大学医学院研究人员确定一个新颖的机制将核醣核酸酸的新陈代谢,RNA,白血病的发展在骨髓增生异常综合征(MDS)患者。在《华尔街日报》发表的一项研究分子细胞造血干细胞,他们解释是什么让获得恶性特征的癌症。
RNA拼接是基因表达调控的主要关系,形成细胞身份在开发期间,经常改变在人类癌症。这个过程是由一个复杂的分子机制称为剪接体,使生产的多个从单个基因和功能上不同的蛋白质。
克里斯蒂安·Bellodi博士领导的研究小组最近发现了一个天生的遗传控制机制调节个体spliceosomal组件,称为剪接因子,细胞内窝藏致癌病变中常见人类癌症。
这项工作突出核心蛋白质剪接,包括SF3B1,经常在各种癌症突变。剪接因子突变在MDS尤其普遍,一群异类血液疾病的特点是有缺陷的造血干细胞和白血病的风险高发展。“越来越多的证据是突出异常剪接的作用在癌症即使没有剪接因子突变。然而,很少有人知道non-mutated剪接因子在肿瘤发展的贡献,”研究人员解释。
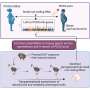
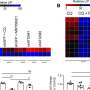
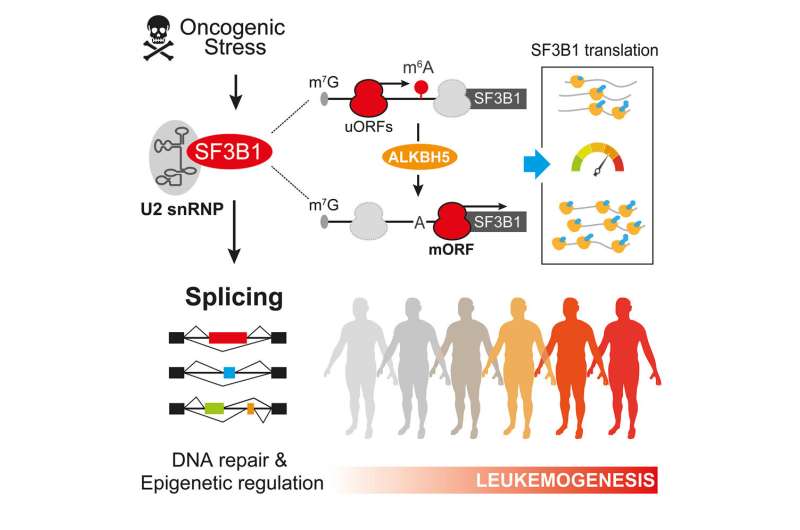
团队开始调查的水平如何non-mutated SF3B1,剪接体的核心组件,导致MDS疾病。与伊娃Hellstrom-Lindberg集团卡罗林斯卡学院教授,Maciej Cieśla和同事发现动态监管SF3B1水平在恶性转变MDS白血病。
“令人吃惊的是,我们发现SF3B1蛋白质积累MDS患者通过剪接调控确保基因组的完整性。阻止这种机制大大加速发展为积极的白血病,”言论Maciej Cieśla,博士后在RNA和干细胞生物学组隆德大学干细胞中心和研究的第一作者,现在IMOL组长,波兰。
作者进一步研究分子的决定因素控制SF3B1生产的过渡时期,白血病。这些研究导致了突破性的发现SF3B1合成取决于一个RNA化学改性马克,称为N6-methyladenosine, m6A,沉积在信使RNA。
“我们发现m6A RNA修改的存在提供了一个停止信号,调节SF3B1生产、关键事件影响DNA损伤的积累白血病细胞”,Cieśla解释说。
“我们的研究结果揭示一个新的关键RNA代谢之间的连接和基因组完整白血病干细胞,提供重要的见解复杂的底层机制推动MDS患者的癌症发展。我们的发现非常及时,因为越来越多的证据表明,RNA修改拼接变化代表新的治疗治疗血液的漏洞和坚实的癌症患者,”克里斯蒂安·Bellodi,副教授,分裂分子血液学和隆德干细胞中心,隆德大学。
更多信息:Maciej Cieśla et al, m6A-driven SF3B1翻译控制引导拼接直接基因组完整性和白血病生成,分子细胞(2023)。DOI: 10.1016 / j.molcel.2023.02.024