新的药物传递方法利用凝血靶向肿瘤
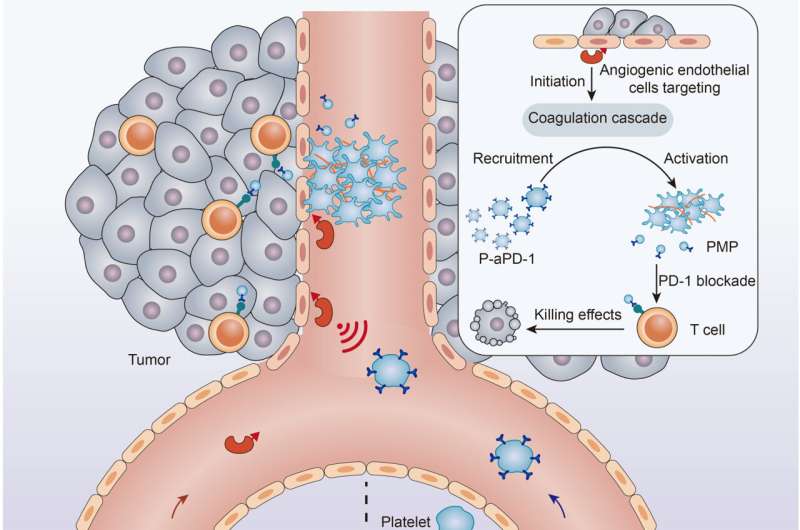
威斯康星大学麦迪逊分校的研究人员开发了一种利用血小板凝血倾向的抗癌药物靶向肿瘤的新方法。
这种新方法最初是在3月29日的杂志上描述的科学的进步威斯康星大学麦迪逊药学院(UW-Madison School of Pharmacy)教授胡泉音(Quanyin Hu)的实验室正在开发一套越来越多的创新给药技术。
他的研究目标之一是提高癌症免疫疗法的有效性和安全性。这种治疗方法通过增强免疫系统的对抗能力而显示出了希望癌症细胞但他们也有自己的挑战。一个重要的障碍是,除了肿瘤外,这些药物还可以靶向正常细胞。这可能会降低治疗效果,有时还会导致严重的副作用。
为了更好地针对肿瘤进行治疗,Hu和他的同事们考虑了一种导致非常特定的生物链反应的机制,即触发血液循环的细胞信号凝块.
“整个研究纯粹是受大自然和血小板自然特征的启发而参与的血栓形成胡说。
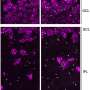
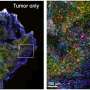
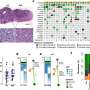
首先,研究人员使用了一种设计用于定位和结合的工程蛋白肿瘤然后在肿瘤内形成血栓或凝血。他们发现,在通过静脉注射接受工程蛋白的小鼠中,蛋白质几乎只在肿瘤内形成凝块,只有非常有限的血栓形成发生在其他地方。
凝块的形成并不是治疗本身,而是为有效、有针对性的治疗创造条件药物输送到充满血块的肿瘤,胡将其描述为“细胞蜂巢”。
“一旦我们在肿瘤部位形成这种凝块,我们就有了这种所谓的细胞蜂巢,可以吸引这些治疗雄蜂,”Hu说。
在这种情况下,无人机是血小板,其表面有免疫疗法,一旦开始凝血,研究人员就会注射。
在他们使用小鼠进行的研究中,Hu和他的同事们发现,经过工程改造的血小板有效地将一种常见的免疫治疗药物——免疫检查点抑制剂——输送到肿瘤部位。检查点抑制剂鼓励免疫细胞也就是T细胞来消灭癌细胞。
与接受传统免疫治疗的小鼠相比,接受这种治疗的结直肠肿瘤小鼠模型的肿瘤缩小,寿命更长。值得注意的是,接受治疗的小鼠中有三分之一完全没有肿瘤。
然后,研究人员用血小板衍生物(包有血小板膜的纳米颗粒并装载化疗药物)在患有人类乳腺癌肿瘤的小鼠模型上测试了这种递送方法。同样,他们发现化疗药物可以有效地传递到肿瘤部位,同时避开正常细胞。这一发现为使用多种药物更有效、更多功能的癌症治疗提供了可能,同时减少了意想不到的副作用。
之前的交付系统可以去临床试验在美国,需要更多的测试以确保其安全性,特别是在凝块形成方面。胡教授说,虽然到目前为止他们在小鼠身上的研究表明,该系统仅在肿瘤部位产生凝块,但下一步将进行更全面的安全性评估。这个过程可能需要几年时间。
更多信息:王宜鑫等,通过肿瘤选择性血栓形成主动招募抗pd -1偶联血小板增强抗癌免疫治疗,科学的进步(2023)。DOI: 10.1126 / sciadv.adf6854.www.science.org/doi/10.1126/sciadv.adf6854