艾滋病治疗的新方向
美国西北大学医学院的科学家们发现了一种新的化合物,可以为未来的艾滋病毒治疗策略提供信息科学的进步.
目前对艾滋病毒感染者的标准治疗是抗逆转录病毒药物,它抑制了艾滋病病毒的传播病毒复制并传播,但不能治愈艾滋病毒。这是因为病毒可以隐藏在免疫细胞内,使自己无法被人体免疫系统检测到,并对抗逆转录病毒疗法产生耐药性。
这种新发现的化合物可以促进一种被称为“休克和杀伤”的实验方法,在此过程中,潜伏的病毒被激活,从而可以被人体的免疫系统或抗逆转录病毒药物靶向。
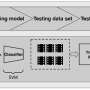
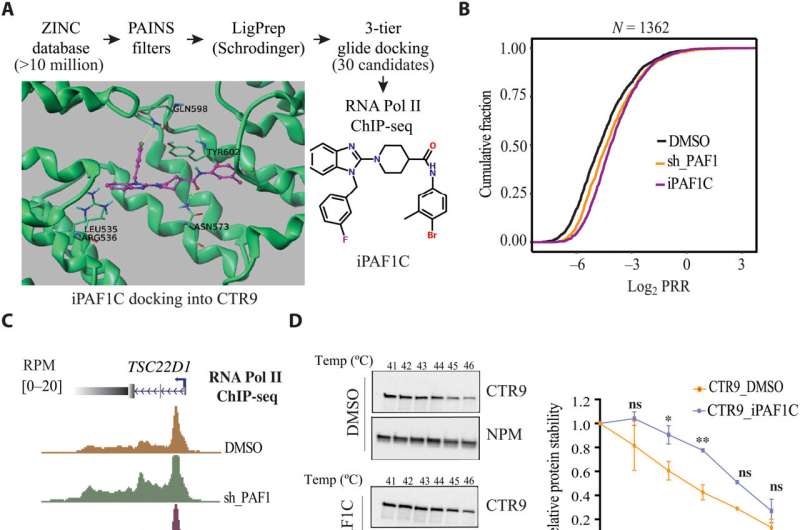
在这项研究中,研究人员利用计算机建模确定了一种抑制聚合酶相关因子1复合体(PAF1C)的化合物,该化合物已被发现在抑制甲型肝炎病毒基因表达中发挥作用先前发表的西北医学研究。
该研究的作者发现,这种被他们命名为iPAF1C的化合物在细胞培养中增强了HIV潜伏期逆转药物的活性。
科学家们还测试了iPAF1C对患者的影响免疫细胞取自四名艾滋病毒感染者的血液。他们发现,虽然这种化合物单独可以激活HIV转录,但与其他延迟逆转药物一起使用时效果最大。
Robert Francis Furchgott教授、生物化学和分子遗传学主席、该研究的资深作者Ali Shilatifard博士说,这种化合物是治疗艾滋病毒的一个有前途的新方向。
“有了这种化合物,我们就有了一些可以调节这些细胞中RNA聚合酶II暂停释放位点的东西,所以我们可以从生物学上研究PAF1调节的暂停释放在不同细胞中的作用,”Shilatifard说,他也是西北大学Robert H. Lurie综合癌症中心的成员,也是该中心癌症表观遗传学和核动力学项目的负责人。“这可能会有巨大的临床应用。”
该研究的合著者、传染病学部医学助理教授贾德·胡尔特奎斯特博士说,这项研究是部门间团队合作的结果。
“这项研究是机构间合作的一个很好的例子,”Hultquist说。阿里提出了利用的想法小分子他和博士后Shimaa在癌症的背景下在我们的一些HIV检测中进行了探索。在第三海岸艾滋病研究中心的支持下,我们能够将这种合作正式化,并在艾滋病毒复制的背景下检查这些蛋白质复合物,结果非常有趣。”
Hultquist说,这一发现也加深了对艾滋病毒潜伏期的理解。
该研究的合著者、德里斯基尔生命科学研究生项目的四年级博士生威廉·西斯内罗斯(William Cisneros)说:“这种化合物可以重新激活潜伏的艾滋病毒感染,这一事实令人兴奋,因为还没有这样的化合物进入临床,所以它可能代表一种逆转潜伏的新策略。”
该研究的作者说,未来的研究将集中于改进这种化合物,以便在动物模型上进行测试。
Shilatifard实验室博士后研究员、该研究的第一作者Shimaa Soliman博士说:“我们正在进一步开发和鉴定更多的iPAF1C化合物,以获得更有效的暂停释放小分子抑制剂,最终的目标是获得临床使用的化合物。”“此外,我们正在测试iPAF1C在治疗其他PAF1起致癌作用的疾病(如癌症)方面的潜力。”
更多信息:Shimaa H. a . Soliman等人,通过调节PAF1C小分子干扰物延长RNA Pol II暂停释放来增强HIV-1潜伏期逆转,科学的进步(2023)。DOI: 10.1126 / sciadv.adf2468