发现新的凝血调节机制
止血对防止失血过多至关重要。然而,如果有过度反应和不受控制的纤维蛋白形成,血栓形成的风险会增加。一项新的研究发表在自然心血管研究来自Würzburg的Bernhard Nieswandt领导的研究小组发现血小板糖蛋白GPV是止血和血栓形成的中心调节因子,这一发现为新的治疗方法开辟了道路。
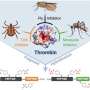
当我们的血管如因割伤、擦伤或擦伤而受伤,止血和包扎伤口是至关重要的。这个过程被称为止血,包括两个主要部分:血血小板附着在伤口边缘,形成一个堵塞,暂时封闭伤口。第二,凝血还是凝血级联被启动,导致长纤维蛋白纤维的形成,它与血小板一起紧密地密封伤口。
然而,如果纤维蛋白形成过多,例如在慢性伤口中,就可能发生血栓形成和随后的血管闭塞。因此,严格调控纤维蛋白的形成非常重要。直到现在,人们还不完全了解凝血是如何受到限制的。
GPV控制凝血酶活性和纤维蛋白的形成
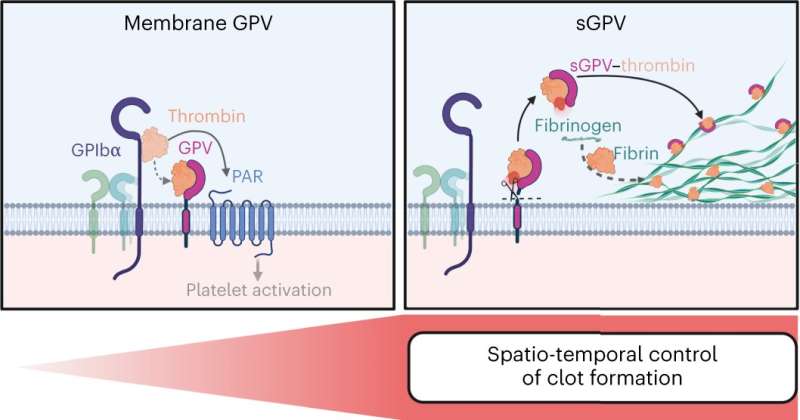
在这项研究中,由Bernhard Nieswandt教授领导的研究小组确定了一种全新的机制。“我们第一次发现了一个新的开关点,可以同时调节止血和血栓形成。这个开关就是糖蛋白V, GPV,它在血小板表面表达。GPV控制凝血酶的活性,凝血酶负责纤维蛋白的形成,”Nieswandt解释说,他是实验生物医学研究所I的负责人,也是Würzburg大学Rudolf Virchow中心-整合和转化生物成像中心(RVZ)的董事会成员。
凝血酶是一种重要的酶凝血因此,它的活动必须在时空上得到精确的控制。到目前为止,已知表面受体GPV在血小板激活过程中被凝血酶裂解。这会以可溶性形式释放GPV。
然而,这种受体的生理功能在很大程度上是未知的。利用遗传和药理学方法,研究人员表明凝血酶介导的GPV裂解限制了纤维蛋白的形成。可溶性GPV通过与凝血酶结合,改变了凝血酶的活性,从而减少了纤维蛋白的形成。
在实验性血栓形成模型中,可溶性GPV被证明可以预防血管闭塞性血栓的形成,并对实验性中风和相关脑损伤产生显著保护作用。
Bernhard Nieswandt相信这些新发现将改变教科书知识。他感谢来自RVZ和大学医院Würzburg (UKW)的所有参与科学家,他们得到了美因茨、马斯特里赫特和美国同事的支持
抗GPV抗体在治疗干扰性止血方面具有巨大的临床潜力
在另一种方法中,研究小组产生了抗GPV的抗体,可以防止凝血酶介导的GPV切割。“在我们的研究中,我们能够证明这些抗体增加凝血酶活性,导致纤维蛋白形成增加。因此,我们的想法是在止血受损的情况下使用这些抗体来增加纤维蛋白的形成,”RVZ血管成像组的负责人、该研究的最后作者之一大卫·斯特格纳教授说。
除了遗传的原因,药物治疗也可导致血小板计数降低或功能受损,从而导致止血功能受损。使用血小板聚集抑制剂治疗,如用于预防心脏病发作或中风和治疗循环系统疾病的氯吡格雷,会损害血小板功能。
“在止血的实验模型中,我们的新抗体确实能够在不可能止血的情况下恢复止血。这表明通过增强凝血酶依赖性来支持止血纤维蛋白该研究的第一作者、Würzburg实验生物医学研究所的科学家萨拉·贝克博士补充道。“抗gpv治疗可能具有巨大的临床潜力。这将在未来进行更详细的调查。”
更多信息:Sarah Beck等,血小板糖蛋白V时空控制纤维蛋白形成,自然心血管研究(2023)。DOI: 10.1038 / s44161 - 023 - 00254 - 6