研究揭示了神经退行性变中脑细胞损伤的驱动因素
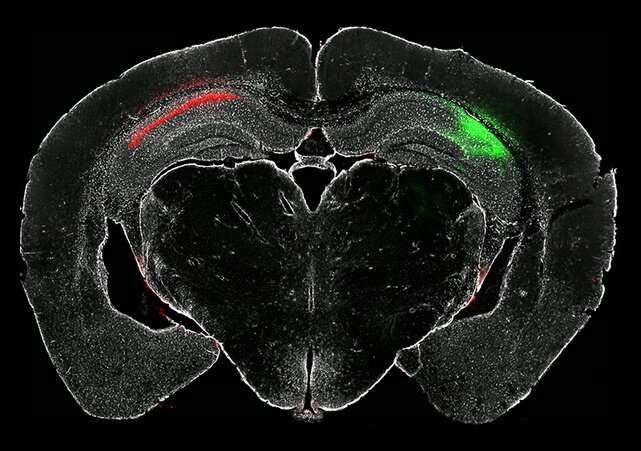
科学家们早就知道,补体级联,一组免疫系统蛋白质,可以防止体内感染。但近年来,研究人员发现了该系统在大脑中的新作用,包括帮助减少脑细胞之间的连接,或突触,以帮助塑造生命早期的神经系统。他们还发现,这一通路在成人大脑中会变得失调,导致阿尔茨海默病和精神分裂症等疾病中的细胞损伤和细胞死亡。但研究人员并不知道这究竟是如何发生的。
由麻省理工学院和哈佛大学布罗德研究所斯坦利精神病学研究中心的科学家领导的一项新研究,确定了成人大脑中第一个已知的补体系统调节器:神经元戊氨酸蛋白Nptx2。Nptx2的缺失使级联不受控制,加剧突触破坏。在神经退行性疾病的模型中,研究人员通过提高Nptx2水平或阻断细胞中的补体蛋白来克服这些影响,这表明针对补体系统的治疗策略可以预防甚至逆转神经退行性疾病对脑细胞的损伤。
这项研究发表在3月29日的《美国医学杂志》上科学转化医学.
该研究的共同资深作者、斯坦利中心的科学家鲍里斯拉夫·德雅诺维奇(Borislav Dejanovic)现在是守夜神经科学的主任,他说:“我们仍然缺乏对究竟是什么因素和事件顺序导致神经退行性疾病的理解。”“像这样的发现帮助我们了解是什么介导了突触的损失和认知能力下降这对病人和他们的家人来说是毁灭性的。”
“这项研究有助于揭示补体级联在一系列神经疾病中的作用,”共同资深作者和Broad核心研究所成员Morgan Sheng说,他也是斯坦利中心的联合主任,麻省理工学院大脑和认知科学系的神经科学教授,以及皮考尔学习与记忆研究所的附属机构。“在斯坦利中心,我们正在努力阐明不同大脑疾病之间的共同机制,揭示意想不到的联系和有希望的治疗途径,有朝一日可能使患者受益。”
Dejanovic和Sheng与john Hopkins大学医学院的神经科学教授Paul Worley一起领导了这项工作。
过度热情的瀑布
在大脑中,补体蛋白结合在突触上,发出“吃我”信号,提醒称为小胶质细胞的免疫细胞吞噬并破坏细胞连接。科学家们推测,这一过程通常在大脑中央受到严格控制神经系统以保护健康细胞免受损伤,但他们还没有在成人大脑中发现任何调节这一途径的分子。
研究人员提出,戊聚糖蛋白家族的成员可能是候选蛋白,因为已知这些蛋白质可以调节身体其他部位的补体活性。科学家们将注意力集中在一种名为Nptx2的戊氨酸蛋白上,它是由兴奋性神经元分泌的,是一系列神经疾病的生物标志物。在阿尔茨海默病患者中,额颞叶痴呆Nptx2在围绕大脑和脊髓的脑脊液中被耗尽。
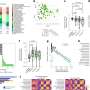
在他们的研究中,研究人员发现Nptx2直接特异性地结合并抑制了补体级联的启动因子C1q的活性。
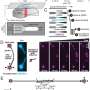
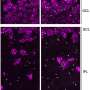
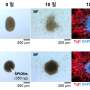
此外,在动物模型缺乏Nptx2,他们发现补体系统的活性增加,同时小胶质细胞破坏突触。当他们通过基因缺失或抗体阻断消除这些动物体内的C1q时,神经元中的突触大脑组织恢复。
在以小胶质细胞过度活跃和补体活性升高为标志的神经退行性疾病动物模型中,促进Nptx2在某些方面的产生大脑细胞导致补体活性下降并逆转突触的丧失。
人为因素
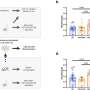
为了测试这种模式是否也会发生在人类身上,研究人员测量了人体中补体和戊聚糖蛋白的水平脑脊髓液来自遗传性额颞叶痴呆患者,在症状出现之前和之后。与症状前基因携带者相比,有症状的患者中C1q和C3b的水平更高,而Nptx2的水平更低。C1q和C3b是级联中进一步激活的补体蛋白。研究小组还观察到,在有症状的患者中,与C1q结合的Nptx2水平降低,这表明大量未结合的C1q可能导致突触丧失并导致痴呆症状。
Dejanovic说:“这些发现有助于解释这种生物标志物的减少是如何导致突触丧失的。”“当Nptx2减少时,补体不再受到限制。”
这项工作支持了抑制补体通路的治疗策略,这有一天可能会改善神经退行性疾病或神经炎症性疾病患者的症状——目前制药行业正在探索这种方法。
与此同时,研究人员将继续探索这种分子系统在健康和其他中枢神经系统疾病(如双相情感障碍)中是如何控制的。
更多信息:周杰超等,神经元五联蛋白Nptx2调节神经退行性变中补体活性及抑制小胶质细胞介导的突触丢失,科学转化医学(2023)。DOI: 10.1126 / scitranslmed.adf0141