研究人员发现双管齐下的方法来刺激STING抗肿瘤活性
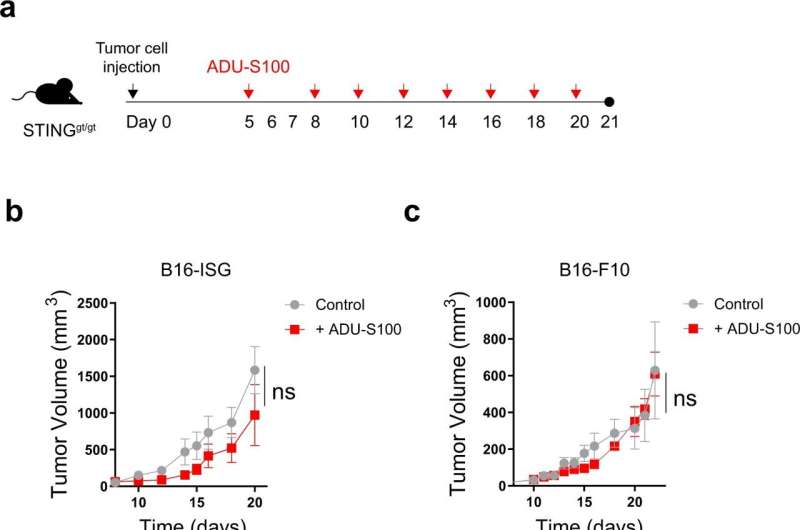
免疫疗法极大地改善了许多黑色素瘤患者的预后。但是,对于那些对这种治疗反应不佳的患者,仍然需要新的治疗方法。莫菲特癌症中心的研究人员正在寻找新的靶点,以帮助抑制肿瘤的发展和促进抗肿瘤免疫,其中一个是STING信号通路。在一篇新文章中发表自然通讯一组Moffitt和迈阿密大学米勒医学院的研究人员证明,以STING通路为靶点的联合策略可提高抗肿瘤活性。
STING通路是对病毒和细菌免疫反应的关键调节因子,并有助于抗肿瘤免疫。STING信号被抑制在几个观察癌症STING蛋白的表达随着某些癌症类型(如黑色素瘤)的进展而减少。这些观察结果表明,激动剂药物,或在肿瘤环境中激活STING信号的药物,可能具有抗肿瘤作用。
“这一假设已在许多临床前实验室研究中得到证实。然而,STING激动剂在人体临床试验中有令人失望的结果,这表明一种未知的机制导致了这些不良反应,”莫菲特免疫肿瘤项目的研究科学家、该研究的主要作者Rana Falahat博士说。“这就是促使我们进行这项研究的原因。”
Moffitt和迈阿密大学的研究小组希望提高他们对STING信号的理解,并研究如何提高STING激动剂的抗肿瘤活性。他们之前证明,控制STING蛋白表达的DNA区域被一种称为甲基化的过程所修饰甲基基团被添加到DNA中。这种修饰降低了STING的蛋白水平,从而减少了STING蛋白的抑制肿瘤发展.研究人员假设,阻断甲基化并增加肿瘤细胞中STING表达水平的药物可能与STING激动剂联合起杀伤作用癌症细胞.
研究人员在肿瘤细胞或周围免疫细胞中STING信号有缺陷的黑色素瘤小鼠模型上进行了实验。与人类的STING基因相似,他们发现小鼠的STING基因也受到甲基化的调控。当研究人员用阻断甲基化的药物处理细胞时,STING的表达和信号传递增加,导致产生增强抗肿瘤免疫的化学信使。他们还证明,用甲基化抑制剂和STING激动剂治疗小鼠可改善抗肿瘤活性,这种活性依赖于被称为CD8 T细胞的免疫细胞的存在和活性。
这些观察结果揭示了重新激活STING信号在脑中的作用肿瘤细胞甲基化抑制剂可以形成STING激动剂的治疗反应。研究人员希望这些临床前的发现将为临床癌症患者带来更好的治疗方法。
“虽然还需要进一步确定每种成分的最佳剂量水平和治疗计划,但我们研究的见解为设计适当的临床治疗模式提供了框架,并对黑色素瘤和其他疾病进行适当的患者选择实体肿瘤James J. Mulé, ip . d说。她是转化科学中心副主任,也是莫菲特黑色素瘤研究和治疗迈克尔·麦克吉利卡迪捐赠主席。
更多信息:Rana Falahat等人,表观遗传状态决定STING激动剂治疗的体内疗效,自然通讯(2023)。DOI: 10.1038 / s41467 - 023 - 37217 - 1