肠道菌群,阿尔茨海默氏症和中枢神经系统
内华达大学拉斯维加斯分校的研究人员已经确定了阿尔茨海默病和特定肠道微生物群之间的相关性。在一篇发表于科学报告题为“阿尔茨海默病和肠道微生物属之间的遗传相关性”,研究人员解释了他们如何将搜索范围缩小到六种与疾病相关的微生物,其中一种与最显著的风险有关。
该研究的作者指出,越来越多的研究表明,常规比例的破坏和肠道微生物群多样性的降低与肠道微生物群的减少有关神经退行性疾病通过微生物-肠道-大脑轴的神经炎症过程。之前的研究也表明,阿尔茨海默氏症患者的微生物群多样性就是这样减少的。
研究人员使用多基因风险评分风险评估根据已知的与疾病的遗传相关性,从1278例病例和1293例对照的发现样本中,每个个体的119个微生物组物种。他们发现119个属中的20个与阿尔茨海默病的诊断显著相关。
在20个重要物种中,6个被确定为可能的风险物种,其他14个被确定为阿尔茨海默病诊断的潜在保护物种。
危险属包括拟杆菌门的阿里氏菌属和拟杆菌属,厚壁菌门的细孔菌属和细孔菌属,放线菌门的柯林斯菌属和假单胞菌门的Sutterella。最显著的风险相关物种是拟杆菌。
在14种保护物种中,有11种来自厚壁菌门,2种来自放线菌门,1种来自拟杆菌门(普雷沃氏菌属9),最显著的保护属为肠杆菌属。
这些发现本身就可以写成一篇有趣的论文,但研究人员似乎对做科学研究更感兴趣,所以他们用后续分析对他们的结果提出了质疑。
第二个数据库来自加拿大阿尔茨海默病患者的多站点合作研究GenADA。同样的技术被用于在799个病例和778个对照组中寻找微生物群之间的相关性。这项复制研究的数据在某些方面与第一次不同,但两个实验在四个显著相关性上重叠,指向了最有可能的罪魁祸首。
APOE4
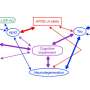
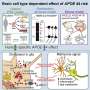
载脂蛋白E (APOE)是中枢神经系统主要的胆固醇和脂质载体蛋白。在APOE2、APOE3和APOE4这三种主要的人类版本中,APOE4的基因表达是与晚发型阿尔茨海默病发展相关的最重要的风险因素之一。
当研究人员深入研究与阿尔茨海默氏症重叠的微生物联系时,他们发现这些患者还有一些有趣的共同点。四种微生物的多基因风险评分与APOE基因型rs429358-C的特定版本有显著相关性。
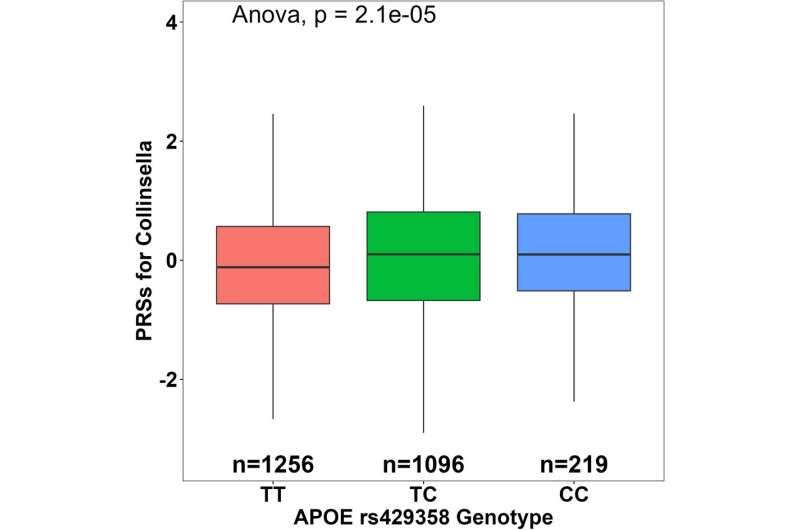
在发现和复制样本中,放线菌门的克林氏菌都被确定为阿尔茨海默病的危险因素,并且与APOE基因型rs429358-C的相关性最显著。
论文指出,先前的研究发现,克林氏菌与较高的血清总胆固醇水平有关低密度脂蛋白(LDL)胆固醇健康的成年人研究人员推测,这可能与科林斯菌和载脂蛋白e之间的相互作用有关。
研究人员得出结论,未来的研究需要探索克林氏菌、脂质代谢和炎症信号之间的关系,以阐明它们的相互作用如何影响阿尔茨海默病和其他疾病。
更多信息:Davis Cammann等人,阿尔茨海默病与肠道微生物群属的遗传相关性,科学报告(2023)。DOI: 10.1038 / s41598 - 023 - 31730 - 5
©2023科学BOB体育赌博X网络