研究人员发现了致命胰腺癌的新治疗途径
约翰霍普金斯金梅尔癌症中心的研究人员发现了一种新的细胞信号传导途径,这种途径可能成为治疗侵袭性胰腺癌患者的靶点。
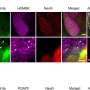
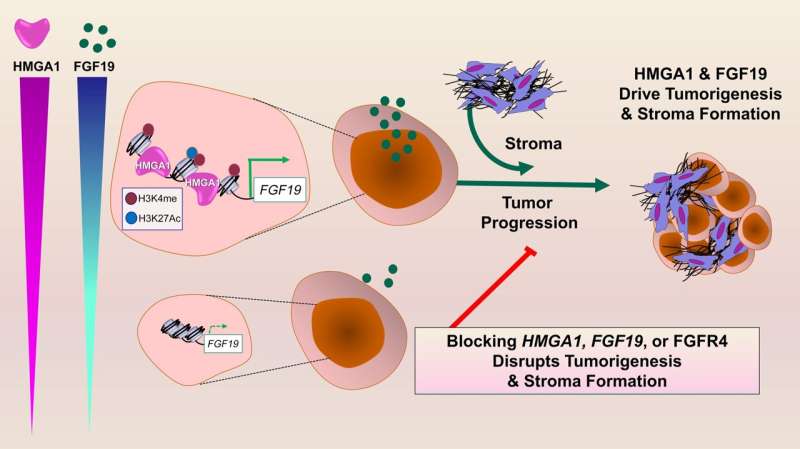
在人类的实验室研究中胰腺癌研究人员发现,高迁移率组A1 (HMGA1)蛋白的功能就像一个“分子开关”,可以“打开”癌细胞所需的基因肿瘤细胞以不受控制的方式和形式生长侵袭性肿瘤。
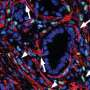
其中一个被HMGA1激活的基因导致成纤维细胞生长因子19 (FGF19)的产生,这是由肿瘤细胞分泌的。FGF19不仅提供信号诱导肿瘤细胞快速生长并侵入周围组织,而且HMGA1和FGF19共同在肿瘤细胞周围“构建”一层致密的、纤维状的、疤痕状的壁,即间质。胰腺肿瘤是少数形成致密间质的肿瘤之一,这种间质被认为会形成一道屏障,阻止治疗到达肿瘤细胞。
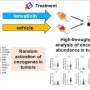
当科学家们在胰腺癌小鼠模型中沉默HMGA1或破坏FGF19信号时,肿瘤细胞的生长明显减少,基质形成减少,这表明阻断FGF19信号的药物已经可用于其他疾病的患者,可以重新用于治疗胰腺肿瘤FGF19含量高对癌症基因组的研究表明,多达四分之一的人类胰腺癌具有高水平的HMGA1和FGF19。
这项工作的描述发表在临床研究杂志。
“胰腺癌是最难治性的肿瘤之一,目前还没有有效的治疗方法,”该研究的资深作者、约翰霍普金斯大学医学、肿瘤学和病理学教授Linda Resar博士说。她说,许多患者在确诊后的6到12个月内死于胰腺癌,基因组数据表明,HMGA1和FGF19水平较高的胰腺癌患者的预后更差,生存期甚至比其他胰腺癌患者更短。
“在之前的工作中,我们发现HMGA1在大多数胰腺癌和非常晚期的前体病变中过表达,以及在其他侵袭性肿瘤如白血病和肝癌中高级阶段骨髓增殖性肿瘤这向我们表明HMGA1在推动肿瘤进展中起着重要作用,”Resar说。
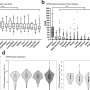
在一系列的实验室实验中,Resar和同事研究了几种破坏HMGA1和FGF19的方法。首先,他们使用短发夹RNA或人工RNA分子阻断原发性和转移性肿瘤的胰腺癌细胞系中的HMGA1基因表达并观察到HMGA1的缺乏会导致生长速度下降,损害迁移、侵袭和其他癌症特性。
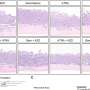
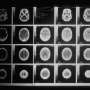
他们还开发了胰腺中缺失一两个HMGA1基因的胰腺癌小鼠模型。令人惊讶的是,仅仅一个基因的缺失就足以减缓肿瘤的形成和发展。
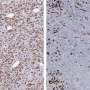
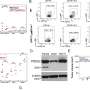
在额外的测试中,研究人员发现FGF19基因的表达、胰腺癌细胞中的蛋白质水平和分泌都依赖于HMGA1。此外,FGF19的沉默也反映了HMGA1的沉默效应,降低了肿瘤的生长和侵袭性。最重要的是,施用BLU9931(一种抑制FGFR4 (FGF19的受体)的小分子药物)导致小鼠肿瘤的肿瘤生长和基质形成减少。
“我们一起发现了我们认为是以前未描述过的范式,即肿瘤细胞通过HMGA1和FGF19协同驱动癌症进展和基质形成,”Resar说。“这项工作还揭示了FGF19作为人类胰腺癌非常侵袭性亚群的潜在治疗靶点。也许我们研究中最令人兴奋的方面是FGF19的抑制剂是可用的,并且已经在人体中进行了测试。”
在正在进行的研究中,研究人员正在评估其他肿瘤,以确定它们是否上调FGF19,并可能从FGF19阻断治疗中获益。研究人员还将测试抑制FGF19是否会阻止肿瘤的扩散或转移肿瘤细胞去遥远的地方。
更多信息:Lionel Chia等,HMGA1诱导FGF19驱动胰腺癌发生和间质形成;临床研究杂志(2023)。DOI: 10.1172 / JCI151601