狗的精确眼部治疗准备用于人类临床发展
密歇根州立大学在患有遗传性眼病的狗身上进行的一项成功的基因疗法试验,准备用于患有罕见疾病色素性视网膜炎的人类患者的临床应用。
Simon Petersen-Jones教授和Donald R. Meyers和William E. Dunlap在密歇根州立兽医学院犬类健康教授,以及他的合作者发表了“cngb1 -色素性视网膜炎的可翻译基因增强疗法的发展”分子治疗。
色素性视网膜炎包括一组罕见的遗传性疾病,由于视网膜中感光细胞的死亡而导致视力丧失。视力丧失始于幼年,并在一生中不断发展。
“目前,对于挽救CNGB1-患者视力的治疗需求尚未得到满足色素性视网膜炎彼得森-琼斯说。“这种很有前途的疗法在狗现在是否已经充分发展到下一步是进行临床试验人类患者。"
克利夫兰诊所估计,全世界大约有200万人患有色素性视网膜炎,其中10万人在美国。目前还没有治愈方法,但这种治疗可能会停止视力丧失对于这种特殊形式的色素性视网膜炎患者。
关于研究
人类和狗共享一种基因——环核苷酸门控通道β 1 (CNGB1),这种基因一旦发生突变,就会导致眼病。狗会患上进行性视网膜萎缩,而人则会患上色素性视网膜炎。
因为基因治疗由于人类会因CNGB1基因突变而发展为视网膜色素变性(相当于狗的视网膜进行性萎缩),该疗法现在已经准备好用于帮助CNGB1视网膜色素变性患者。
彼得森-琼斯说:“我们非常希望这种疗法能在人类临床试验中显示出与狗相同的积极结果,并导致fda批准的cngb1色素性视网膜炎的成功治疗。”
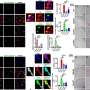
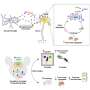
在这项研究中,彼得森-琼斯使用一种腺相关病毒(AAV)载体,在一种新的基因启动子的控制下,传递了CNGB1基因的正常拷贝。这种新型启动子是由Petersen-Jones的合作者开发的,是人类视紫红质启动子的修饰形式,视紫红质是视网膜杆状细胞中的一个重要基因。这种新型启动子确保了由治疗剂引入的CNGB1仅在靶细胞-视杆光感受器中具有活性。
该AAV为5型血清型,包装有短视紫红质启动子CNGB1基因组合(AAV5-RHO-CNGB1)。这种疗法是在视网膜下注射的,这样它就会被引入到目标光敏杆状细胞中,这些细胞需要正常的CNGB1来发挥作用和存活。
治疗:
- 通过引入CNGB1的正常工作拷贝,恢复杆状细胞的正常功能并恢复杆状细胞介导的视觉
- 停止在正常功能的杆状细胞中积累有毒的环鸟苷单磷酸,如果不减少,会导致细胞死亡
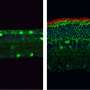
- 保留视锥细胞功能——在未经治疗的眼睛中,视锥细胞会随着视杆细胞的死亡而消失
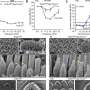
- 通过阻止光感受器变性来保护视网膜结构
这项研究涉及来自8个国际机构的20位作者,包括学术界和工业界。他们的发现确立了基因疗法的长期疗效,并且是先前的研究。
更多信息:Laurence M. Occelli等,cngb1 -色素性视网膜炎的可翻译基因增强疗法的发展,分子治疗(2023)。DOI: 10.1016 / j.ymthe.2023.04.005