临床前研究确定复发性卵巢癌的新靶点
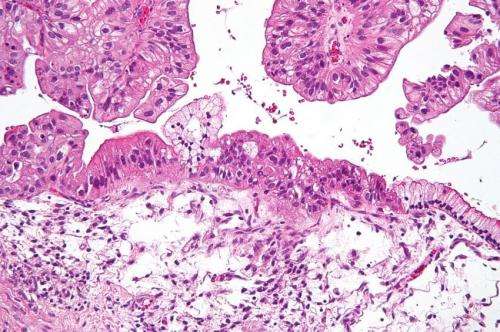
尽管最近取得了一些进展,但卵巢癌仍然是导致女性癌症相关死亡的第五大原因,迫切需要新的治疗方案,特别是在标准护理治疗后复发的晚期癌症。宾夕法尼亚大学佩雷尔曼医学院的研究人员领导的一项临床前研究的结果,验证了耐药卵巢癌的一个新靶点,并为支持一种已经进入临床试验的治疗方法提供了数据。
Sarah Gitto博士,病理学和实验室医学讲师,将在2023年美国癌症研究协会(AACR)年会上介绍这些发现(摘要#1133)。
“不幸的是,大多数人卵巢癌复发并对标准铂化疗产生耐药性,”资深作者、医学博士、妇产科教授菲奥娜·辛普金斯说。“Platinum-resistant卵巢癌最具挑战性的卵巢类型是什么癌症治疗和开发这一领域的新疗法是当务之急。”
PARP抑制剂(PARPi)是一种新型的靶向标准护理治疗,可提高患者的生存率卵巢癌患者但是,与化疗类似,这些疗法最终对许多患者无效,使他们没有治疗选择。
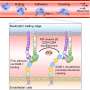
为了应对这些挑战,这项研究将重点放在蛋白质B7-H4上,作为合著者和合作者,病理学和实验室医学副教授Daniel J. Powell Jr.博士的关键工作表明,它是一种潜在的高影响靶点,在大多数乳腺癌和卵巢癌诊断中发现。由于癌症治疗可以影响细胞上表达的蛋白质,研究人员开始确定B7-H4在反复治疗后是否仍然高水平表达,因此对于已经接受化疗或PARPi的患者来说,B7-H4是一个合适的靶点。
研究小组使用了来自宾夕法尼亚卵巢癌研究中心肿瘤生物信托收集的匹配样本,以观察在治疗前、治疗中和治疗后,在同一患者的肿瘤组织中是否发现了B7-H4,在某些情况下,在终末期转移性疾病的设置中。他们发现,在诊断时分析的92%的高级别浆液性卵巢癌(HGSOC)肿瘤中,B7-H4过表达,并在整个癌症治疗过程中保持高水平,甚至在化疗或PARPi之后。重要的是,这种蛋白质始终存在于细胞外部(而不是仅仅存在于细胞外部)内部细胞),药物可以很容易地与细胞结合。
抗体-药物偶联成功靶向B7-H4
在确定B7-H4作为可行的靶点后,研究人员在多个细胞系和20多个患者来源的乳腺癌和卵巢癌异种移植瘤(PDX)模型中测试了抗体-药物偶联物。抗体-药物偶联物是一类新的高度靶向的免疫治疗药物,其毒性远小于传统的化疗。
在没有接受过任何PARPi或化疗的PDX模型中,61%的肿瘤在一次剂量后体积减小。通过每28天继续治疗,以更好地模拟临床给药,该药物导致显著的肿瘤消退,并增加患者的生存率治疗-抗PDX模型。
“我们看到了出色的抗肿瘤活性,在模型中持续了很长一段时间耐药这并不常见,”吉托说。“我们已经能够证明B7-H4是一个非常强大和广泛的靶点,可以在患者护理的多个阶段使用。”
一种靶向B7-H4的抗体-药物偶联物目前正在进行一项多位点I期临床试验(NCT05123482)。
“我们对它的潜力感到兴奋抗体药物配合来克服耐药性,这项工作表明它们值得在卵巢癌中进一步发展,”Simpkins说。“这种类型的进展是可能的,这要感谢参与研究的患者,包括生物标本库项目,让科学家了解他们的疾病如何随着时间的推移而变化。”
Gitto在4月16日星期日的创新治疗方法迷你研讨会上介绍了这一发现。
更多信息:抽象的# 1133