新工具有助于临床解释遗传信息
尽管在临床实践中越来越多地使用基因组测序,但解释罕见的基因突变,即使是在研究充分的疾病基因中,仍然很困难。目前的预测模型对解释这些突变很有用,但它们容易对那些不会引起疾病的突变进行错误分类,从而导致假阳性。
来自德累斯顿马克斯普朗克分子细胞生物学和遗传学研究所(MPI-CBG)、德国德累斯顿系统生物学中心(CSBD)和美国波士顿哈佛医学院的研究人员开发了一种名为破译可操作基因突变(DeMAG)的工具。这项研究发表在杂志上自然通讯。
DeMAG是一个开源网络服务器(demag.org),它提供了316例临床相关病例中可能发生的所有潜在单氨基酸突变的解释基因导致预防性诊断和治疗已经可用的疾病。DeMAG为医疗专业人员提供了一种工具,通过降低假阳性率,使他们能够更准确地评估这些基因突变的影响,这意味着不太良性的突变被预测为致病的。因此,该工具可以支持临床决策。
近年来,基因组测序变得越来越便宜和先进。一方面,这允许临床医生越来越多地将测序用于诊断目的,同时也允许科学家探索更多的研究假设。另一方面,许多检测到的突变没有明确的临床解释。突变是否导致疾病的不确定性可能给患者带来压力,并导致与诊断不足和过度诊断相关的心理负担、发病率和医疗保健费用。
虽然现有工具已经用于预测这些变异的功能影响,但由于有限的临床数据使得区分给定基因内的致病性(致病)和良性(中性)变异变得困难,并且经常导致将不致病的突变错误分类为致病性,因此它们的表现存在偏差。解决这些困难对于开发临床应用的可靠预测器至关重要。
MPI-CBG和CSBD的Agnes Toth-Petroczy研究小组与哈佛医学院布里格姆妇女医院遗传学部的医学助理教授克里斯托弗·卡萨(Christopher Cassa)和哈佛医学院生物医学信息系的研究助理伊万·阿德朱贝(Ivan Adzhubei)合作,开发了一种新方法统计模型以及网络服务器DeMAG,它在解释疾病基因的基因突变方面达到了很高的准确性。为了做到这一点,研究人员仔细选择了已知的致病和良性突变来训练模型。
“我们使用了临床和各种人口数据库。我们只选择临床解释在多个提交者(如医生和遗传学实验室)之间达成一致的突变。我们还包括了目前人口数据库中代表性不足的祖先的数据,比如韩国人或日本人,以使其更具代表性和准确性,”该研究论文的第一作者、tot - petroczy小组的博士生Federica Luppino解释说。
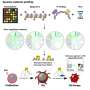
DeMAG包含了一个新颖的特征,“伴侣评分”,它可以识别蛋白质中具有相同临床效果的氨基酸簇。根据合作伙伴的得分,DeMAG利用了基于许多生物体基因组进化信息的氨基酸关系,以及最近使用b谷歌DeepMind开发的AlphaFold算法预测蛋白质3D形状的人工智能(AI)革命。
监督这项研究的Agnes Toth-Petroczy总结道:“我们为整合临床和蛋白质数据提供了一个基本框架,以帮助评估药物的影响突变。我们希望我们的工具和web服务器将简化变异效果评估和临床决策。此外,新开发的特征可以应用于人类以外的其他基因和生物体。”DeMAG代码可在GitLab (git.mpi-cbg.de / tothpetroczylab / DeMAG),所有资料均可免费在网页伺服器(网址demag.org/。
更多信息:Federica Luppino等人,DeMAG通过整合结构和进化上位性特征来预测临床可操作基因变异的影响,自然通讯(2023)。DOI: 10.1038 / s41467 - 023 - 37661 - z