一个难以捉摸的消耗综合征恶病质披露机制
部门的研究人员Koc大学分子生物学和遗传学在土耳其和内分泌学的钢管,糖尿病学和营养、大学研究所的实验和临床研究Catholique de比利时鲁汶合作审问一个癌症相关的浪费syndrome-cachexia背后的机制。
摘要“EDA2R-NIK信号促进肌肉萎缩导致癌症恶病质,”发表在自然、细节的发现有一个可变剪接ectodysplasin (EDA)导致信号通路在恶病质病理学。一个新闻和观点相同的轮廓》期刊上发表的研究结果。
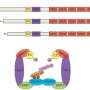
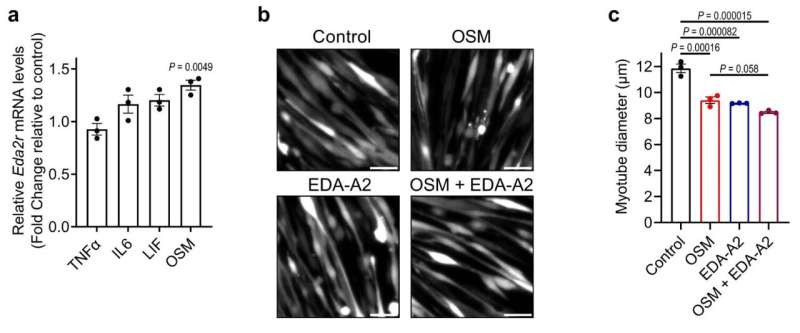
EDA,类型的细胞因子,属于肿瘤坏死因子(肿瘤坏死因子)信号蛋白超家族,由白细胞免疫系统要做的工作。研究人员发现,EDA的可变剪接,EDA2R信使RNA,是丰富的骨骼肌组织与消耗综合征恶病质小鼠。
消耗综合征
恶病质最常出现在胰腺癌和先进肺癌和经常与结直肠、卵巢和肝脏的癌症。
定义为下跌5%或更多的体重在前六个月中,恶病质也能导致疲劳和强度降低。的定义本身是一个粗略的衡量标准更复杂的生理条件,可以在诊断为癌症治疗可以有重叠类似的效果。
物理与恶病质可以加速萎缩病人可能无法执行常规任务,如洗澡,购物或喂养自己,缺乏体力或没有食欲。心理健康问题会很快跟进。此外,恶病质的影响被认为是直接的因果近三分之一的癌症死亡时心脏或呼吸衰竭由于肌肉损失发生。
没有已知的机制,即使诊断有限可以使用没有有效的治疗方法,在临床设置一个明确的行动。
有趣的相关性
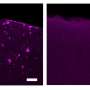
通过基因表达搜索肌肉活检,研究者发现高架EDA2R mRNA恶病的患者癌症(肺癌、胃肠、胰腺和结肠直肠癌)相比,癌症患者没有恶病质和癌症控制。
此外,研究小组发现,患有降低肌肉和功能与杜氏营养不良症肌肉萎缩症(DMD)和facioscapulohumeral肌肉萎缩症(FSHD)也显著升高EDA2R成绩单。
与EDA-A2-EDA2R通路相关检测,研究人员进一步进行调查。
发现机制
从组织文化和推进小鼠模型,团队多次发现增强EDA-A2蛋白质含量产生了有害的影响。他们观察细胞大小减少组织培养和体内小鼠实验显示的肌肉退化。
实验还显示下游EDA-A2受体相互作用后的影响。NFĸB-inducing激酶(尼克)转录因子调控的重要控制大量的基因的表达,是启动激活基因转录酶能分解肌肉组织。
上游的受体EDA2R表达式,研究人员发现肿瘤导致制瘤素M (OSM)作为一个关键调节器。损耗OSM信使RNA的肌肉保护他们反对浪费和萎缩。
研究结果表明,OSM-OSMR信号行为与EDA2R-NIK并行通路和强化肌肉萎缩和EDA2R upregulation。
删除EDA2R或尼克在老鼠足以赋予抵抗肿瘤导致肌肉萎缩。作者建议针对OSM-OSMR途径也可能是一个高价值的治疗目标。
与任何良好的学习,更多的研究是必要的。接下来的步骤可能会确定哪些目标保持最好的风险-效益比率和推进对临床干预对因果关系的理解。
更多信息:Sevval努尔Bilgic et al, EDA2R-NIK信号促进肌肉萎缩导致癌症恶病质,自然(2023)。DOI: 10.1038 / s41586 - 023 - 06047 - y
劳拉Antonio-Herrera et al,对肌肉的损失导致恶病质,分子基础自然(2023)。DOI: 10.1038 / d41586 - 023 - 01527 - 7
©2023科学BOB体育赌博X网络