研究人员观察肠道刺激癌症免疫疗法的战斗力量

癌症免疫疗法改变了许多类型的癌症的治疗。然而,仍然了解甚少的原因,不是所有的病人得到相同的从这些强大的治疗中获益。
治疗效果的一个强有力的因素似乎是一个人的肠道microbiota-the数以万亿计的微生物生活在人类intestine-according新的研究由哈佛医学院研究人员和丹娜-法伯癌症研究所。
这项研究在老鼠和发表在5月3日完成自然,发现肠道微生物如何增强机体免疫反应的一个常见的一种免疫疗法称为PD-1检查站封锁,目前用于治疗25形式的癌症。
调查发现,特定的肠道细菌会影响两个的活动吗免疫分子-PD-L2和RGMb-as以及它们之间的相互作用。
工作还表明,阻塞的活动分子或它们之间的相互作用增强的反应癌症免疫疗法和优化探测和摧毁身体的能力癌症细胞。
“PD-L2之间的接触和RGMb作为制动抗癌T细胞,和我们的工作表明,治疗用抗体块之间的相互作用与RGMb PD-L2释放刹车和T细胞可以消除肿瘤,”文章的第二作者阿琳夏普说,Kolokotrones大学哈佛大学教授和系主任的免疫学HMS Blavatnik学院。
夏普共同研究与丹尼斯·卡斯帕威廉埃勒里钱宁的医学教授和HMS免疫学教授,医学教授和戈登弗里曼HMS和dana - farber。
研究还确定了分子RGMb作为一个前所未知的共犯破坏体内的能力发现并摧毁肿瘤。RGMb,主要以其作用在神经系统开发中,也发现抗癌T细胞表面。然而,直到现在,没有人知道它扮演了一个角色在调节t细胞对癌症免疫疗法的反应。
如果复制人类,这些发现可以通知疗法的设计,改善免疫疗法治疗结果,研究人员指出。
“我们的发现提供了一个重要线索为一个复杂难题,从而提出具体的方法来提高癌症免疫疗法的效力和改善病人的结果,”研究作者co-first俊Seok公园,夏普在免疫学实验室做博士后研究。“我们提出一个新的方法来克服阻力当前癌症免疫疗法的肠道细菌,帮助我们的学习免疫系统对抗癌症。”
癌症如何躲避免疫检测和破坏
癌症的生存和传播的关键是其逃避人体免疫防御的能力。从1990年代开始,夏普和弗里曼执行的一些关键的早期作品,阐明癌症如何管理。
夏普和弗里曼的工作主要集中在两个分子,PD-L1 PD-L2,驻留在免疫细胞的表面。他们的研究表明,当PD-L1或PD-L2与另一个分子,PD-1,表面上的T细胞,T细胞的活性保存在检查。在正常情况下,这种交互功能抑制T细胞,以确保他们不会错误地攻击人体自身的细胞和组织。
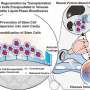
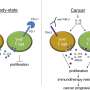
夏普,弗里曼和其他人发现癌症利用正是这种安全机制逃避检测T细胞和破坏。癌细胞通过表达PD-L1和PD-L2表面,与PD-1和抑制T细胞。癌症免疫疗法的交互块PD-1 PD-L1或PD-L2释放T细胞的攻击癌症和被称为免疫检查点封锁。
这种治疗方法,目前用于25癌症,革新了癌症治疗,但病人不受益于他们的一个子集。从这些疗法的出现以来,研究人员一直试图理解为什么。
免疫系统之间的相互作用和肠道微生物群Kasper多年的工作的重点。他的实验室已经确认不仅监管机制,而且特定的微生物和微生物分子酶负责调节免疫系统。
肠道微生物的观念可能影响癌症免疫疗法并不是全新的。最近的研究已经发现了一些振奋人心的线索对肠道微生物的作用在免疫疗法治疗结果。然而,直到现在,一个关键问题仍未得到回答:怎么了?
新玩家进入现场
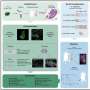
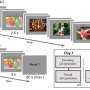
在新的研究中,研究人员用老鼠的冒号被播种癌症患者的肠道微生物群。一些患者的免疫治疗反应良好,而其他人没有经历太多的好处。这些动物的反应免疫疗法的治疗反应模仿人类的肠道微生物现在住在他们的肠子。
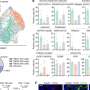
比较两组老鼠的免疫系统资料,研究人员发现的差异在不同的免疫细胞参与癌症检测和破坏。这一发现表明,肠道微生物群改变免疫细胞的行为,因此,应对免疫疗法。
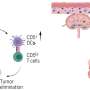
小鼠的肠道微生物与癌症病人自己反应良好的免疫疗法PD-L2水平较低的类被称为抗原递呈细胞的免疫细胞。这些细胞在团结发挥关键作用人体的免疫防御。他们通过巡逻体内病原体或肿瘤和呈现这些外国或异常蛋白质为杀伤性T细胞。相反,小鼠的肠道微生物与患者不良反应免疫疗法增加了PD-L2分子水平。
梳理出特定的肠道微生物的影响,研究人员组小鼠与广谱抗生素治疗,杀死肠道细菌。Antibiotic-treated老鼠没有回应免疫疗法,封锁了PD-1分子。然而,这些老鼠有高水平的PD-L2,其它分子刹车,通常通过PD-1行为。动物有一个健壮的反应相同的治疗PD-L2水平较低。
好奇,PD-1封锁不工作,研究人员推测,PD-L2作为抑制T细胞,而不是仅靠PD-1通过另一个分子的帮凶。研究者将注意力转向RGMb,弗里曼实验室先前表明RGMb和PD-L2监管在肺部免疫耐受。
当科学家把老鼠没有回应anti-PD-1疗法单独与抗体RGMb阻塞,这些动物经历了抗癌T细胞的增加和快速的整体改善。
“微生物群之间的相互作用和免疫细胞的抗癌响应刚清晰,和识别RGMb PD-L2分子的帮凶,我们有另一个癌症免疫疗法的目标,”弗里曼说。
进一步的分析表明,RGMb之间的交互和PD-L2取决于肠道微生物的组成。研究人员发现,某些肠道微生物可能影响两分子的水平。
小鼠的肠道已经播种与某些癌症肠道微生物已经六次RGMb在T细胞水平低于无微生物的动物内脏和回应anti-PD-L1或anti-PD-1疗法。相比,小鼠枯竭的肠道微生物群没有回应这些治疗和更高水平的RGMb T细胞,尤其是在T细胞渗透到他们的肿瘤。
同样,小鼠的肠道被播种的微生物群贫困患者治疗反应也有更高水平的RGMb,发现表明病人不挂载一个好的应对癌症免疫疗法港更高水平的RGMb T细胞,进而干扰免疫细胞的抗肿瘤反应。
禁用的活动或者PD-L2 RGMb足以保护T细胞的抗肿瘤活性和确保一个健壮的应对PD-L1和PD-1疗法。值得注意的是,阻止PD-L2的活动导致了强有力的抗肿瘤反应动物对待另一种形式的癌症免疫疗法被称为树突细胞疗法。观察表明,调制PD-L2活动持有承诺提高应对多种类型的癌症免疫疗法。
肠道微生物免疫反应的监管机构
改变肠道微生物群的组成在不同组的老鼠显示一个有机体,c . cateniformis抑制PD-L2水平和呈现在小鼠癌症免疫疗法更有效。
鉴于人类肠道是成千上万的细菌物种,这微生物可能不是唯一的生物调节抗肿瘤免疫的能力,研究人员说。
发现表明,特定的微生物分子可以利用小分子药物的形式来增强免疫系统控制癌症的能力。这种治疗方法可以补充或替代传统的基于抗体的癌症免疫疗法。
小分子的方法,还可以开发和商店更便宜的吸引力,更容易传递到身体,夏普说。小分子药物通常是作为药物,而癌症免疫疗法给杰克逊静脉注射的方式注入抗体。
研究人员警告说,尽管他们的工作揭示了一个关键的难题,很可能只有一个免疫系统的几种方法和微生物相互作用的癌症。
“这可能只是故事的开始,“弗朗西斯卡Gazzaniga说co-first作者研究前Kasper实验室的博士后研究员,他现在的病理学副教授HMS和麻省综合医院的首席研究员。“癌症、免疫系统和微生物单独数量惊人,但当你把这些系统在一起,由此产生的相互影响是指数更复杂。”
“可能有许多其他方式一般微生物可以影响癌症免疫和癌症免疫疗法特别是,”卡斯帕说。“有了这个工作,我们发现了一个全新的观察方式肠道微生物群不仅影响癌症治疗的疗效癌症免疫力。”
更多信息:丹尼斯·卡斯帕,目标PD-L2-RGMb克服microbiome-related免疫治疗抵抗,自然(2023)。DOI: 10.1038 / s41586 - 023 - 06026 - 3。www.nature.com/articles/s41586 - 023 - 06026 - 3