底层机制和潜在的治疗神经性疼痛的目标
神经性pain-abnormal过敏刺激与生活质量受损,往往是管理不善。估计表明,3%到17%的成年人患有神经性疼痛,包括四分之一的糖尿病患者和艾滋病毒携带者的三分之一。
在《华尔街日报》发表的一篇论文神经元,研究人员报告说,一种机制涉及酶Tiam1脊髓背角兴奋性神经元的启动和维护神经性疼痛。此外,他们表明,针对脊髓Tiam1与反义寡核苷酸注入脑脊液有效缓解神经性疼痛过敏症。
“因此,我们的研究发现了一个病理生理机制,提升者,转换和维持神经性疼痛,我们已经确定了一个有前途的治疗目标治疗神经性疼痛与持久的后果,”Lingyong李说,博士,副教授伯明翰阿拉巴马大学麻醉学和围手术期药物。“了解神经性疼痛的病理生理机制是至关重要的发展新的治疗策略来有效治疗慢性疼痛。”
李和金伯利Tolias博士休斯顿贝勒医学院的教授,德克萨斯州,变的研究。
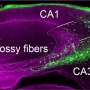
这是知道神经性疼痛的一个特性是不适应的改变神经元的脊髓背horn-increases树突棘的大小和密度,主要的兴奋性突触的突触后的网站。然而,推动这种机制突触可塑性都不清楚。树突是树状附属物附着在身体的神经元接收来自其他神经元的通信。脊髓背角的脊髓的三个灰色的列。
在相关工作去年,李和Tolias发现,慢性疼痛小鼠模型导致一个激活Tiam1前扣带皮层锥体神经元的大脑,导致神经树突棘的数量增加。这更高的脊柱密度增加的连接数,这些连接的强度,神经元之间,被称为突触可塑性变化。那些增加引起的超敏反应联系在一起慢性疼痛在小鼠模型有关的抑郁症。
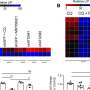
当前的神经性疼痛研究李和Tolias使用小鼠模型引起的神经性疼痛神经损伤、化疗或糖尿病。研究人员表明,Tiam1激活脊髓背角的老鼠受到神经性疼痛,Tiam1全球基因敲除小鼠预防神经性疼痛的发展。全球淘汰赛导致没有其他明显异常的老鼠。
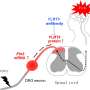
UAB和贝勒研究者发现Tiam1表达在脊髓背角neurons-but不是背根神经节神经元或兴奋前脑neurons-was神经性疼痛的发展至关重要。此外,他们发现神经性疼痛发展取决于Tiam1表达抑制性神经元的兴奋性神经元没有。
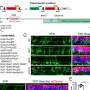
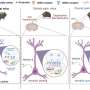
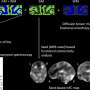
显示Tiam1行为在神经性疼痛后,李,Tolias和同事显示Tiam1做什么。Tiam1已知调节其他蛋白质的活动,帮助建立或摧毁的骨骼细胞,和细胞骨架肌动蛋白细丝的建筑是树突棘创造的一部分。研究人员发现Tiam1神经性疼痛的开发过程中需要增加树突棘的密度宽动态范围从脊髓背角神经元,增加突触NMDA受体脊髓背角神经元的活动。
Tiam1功能激活小GTPase Rac1酶,促进肌动蛋白聚合。研究人员表明,Tiam1-mediated神经性疼痛的发展依赖Tiam1-Rac1信号。然后用小分子抑制剂阻止Rac1激活在三个不同的时间点周围神经损伤后,四天神经损伤后神经性疼痛过敏逐渐发展,或三周后神经损伤,慢性神经性疼痛完全建立。他们发现,神经性疼痛是预防或逆转在每个时间点。因此,Tiam1-Rac1起始信号是至关重要的,转换和维护神经性疼痛。
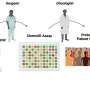
自从Tiam1似乎是一个有前途的治疗目标治疗神经性疼痛,李和Tolias还测试了是否可以减少注射反义寡核苷酸的神经性疼痛,或ASOs-short,合成,单链oligodeoxynucleotides旨在改变Tiam1表达式通过调节其mRNA加工或degradation-into脊柱的脑脊液。
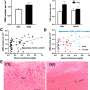
注射在大鼠模型中,他们发现一个麻生太郎对Tiam1脊髓背角Tiam1蛋白质水平降低了50%,明显减少了神经性疼痛超敏反应注射后一周,减少又多持续了两周。
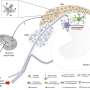
因此,Tiam1的发病机制是一个重要的球员神经性疼痛肌动蛋白细胞骨架动态坐标,树突棘的形态发生和突触受体功能脊髓背角神经元兴奋性神经损伤,李和Tolias说。
更多信息:李Lingyong et al, Tiam1坐标突触结构和功能可塑性神经性疼痛的病理生理学基础,神经元(2023)。DOI: 10.1016 / j.neuron.2023.04.010