新的研究表明谷氨酰胺酶2在胰岛细胞调节葡萄糖代谢
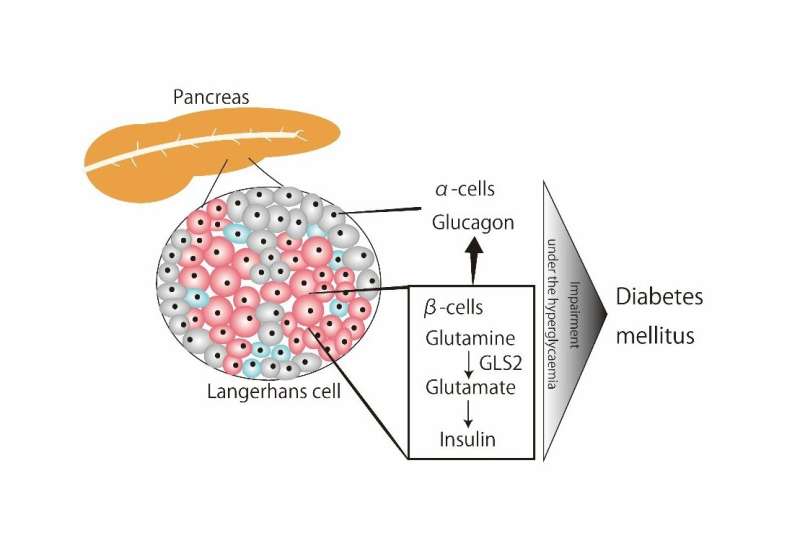
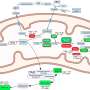
谷氨酰胺酶2 (GLS2)是glutaminolysis主监管机构。GLS2谷氨酰胺转化为谷氨酸,从而发挥作用在细胞能量生产。GLS2丰富在肝脏,还发现在胰腺β-cells。然而,GLS2的角色在胰腺小岛ɑ-和β-细胞与葡萄糖代谢present-associated目前未知。
葡萄糖稳态是由一个错综复杂的交互之间的肝脏,胰腺ɑ-细胞(使胰高血糖素),胰腺β-cells(使胰岛素)和相关的器官,如肠道、骨骼肌和脂肪组织。
日本千叶大学的研究人员曾认为GLS2目标基因p53,从而作为一个肿瘤抑制功能。由于糖尿病和癌症密切相关,他们决定进一步检查的作用β-cells-specific GLS2葡萄糖稳态。
在目前的研究中,他们发现了GLS2葡萄糖体内平衡的作用。他们通过使用小鼠模型,GLS2在胰腺β-cells有条件地删除,被称为GLS2 CKO老鼠,连同人类胰岛基因数据存储库。他们的研究结果发表在网上科学报告。这项研究是由汉娜Deguchi-Horiuchi女士,一个博士生,高级讲师Sawako铃木和由教授Koutaro Yokote千叶大学。
“我们以前的工作确定GLS2 p53的目标,控制ferroptosis,和显示GLS2体内肿瘤抑制功能。我们也知道GLS2谷氨酸的代谢调控分子胰岛素生产和推测,这种酶葡萄糖体内平衡的作用胰腺胰岛。这项研究提供了重要的见解作为糖尿病和癌症可能共享一个共同的发病机制的分子基础,”铃木博士解释道关于集团追求的动机研究。
研究团队相比葡萄糖稳态之间Gls2淘汰赛(Gls2 CKO)和控制(RIP-Cre)老鼠。
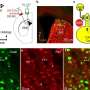
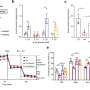
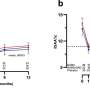
“当美联储高脂肪饮食,我们发现GLS2和p53表达增加胰腺β-cells RIP-Cre老鼠。相反,Gls2 CKO老鼠了糖尿病葡萄糖、胰岛素抵抗和持续生产。矛盾的是,胰岛素分泌镇压,胰高血糖素分泌尽管高血糖水平升高在Gls2 CKO老鼠,”铃木博士说。“这表明受损GLS2活动推动糖尿病的发病加剧破坏胰岛素和胰高血糖素的监管。”
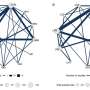
研究小组的研究结果验证了在不同的实验中GLS2沉默在胰腺β-cells来自老鼠细胞系。再次,胰岛素分泌减少。此外,人类胰岛细胞基因表达糖尿病捐助者的数据显示增加GLS2表达式。最后,符合Gls2基因敲除小鼠数据,表达下调Gls2糖尿病患者的胰腺β-cells捐助者是矛盾与抑制胰岛素和胰高血糖素基因表达增强有关。
这些发现表明胰腺β-cell GLS2复杂参与调节血糖水平条件下的高血糖。但有什么长期治疗应用这项研究?
事实上,这项研究强调发展中特制的糖尿病药物必须结合患者的血液遗传信息和数据葡萄糖水平,代谢状态、年龄、糖尿病、持续时间和疾病的家族史。
铃木博士总结道,“我们需要深入了解GLS2-regulated葡萄糖代谢。病人窝藏GLS2丧失基因改变可能本身就有可能发展为糖尿病。在未来,GLS2甚至可以从这个衰弱性疾病患者的治疗目标。”
更多信息:汉娜Deguchi-Horiuchi et al,胰腺β-cell谷氨酰胺酶2维持葡萄糖稳态条件下的高血糖症,科学报告(2023)。DOI: 10.1038 / s41598 - 023 - 34336 - z